Estado de la materia
Definición
En física, el estado de la materia es una de las formas distintas en que la materia puede existir. Cuatro estados de la materia son observables en la vida cotidiana: sólidos, líquidos, gaseosos y plasmáticos. Se sabe que existen muchos otros estados, como vidrio o cristal líquido, y algunos solo existen bajo condiciones extremas, como condensados de Bose-Einstein, materia degenerada por neutrones y plasma de quark-gluón, que solo se producen, respectivamente, en situaciones de frío extremo, densidad extrema y extremadamente alta energía. Se cree que algunos otros estados son posibles pero siguen siendo teóricos por ahora. Para obtener una lista completa de todos los estados exóticos de la materia, consulte la lista de estados de la materia.
Históricamente, la distinción se basa en diferencias cualitativas en las propiedades. La materia en estado sólido mantiene un volumen y forma fijos, con partículas componentes (átomos, moléculas o iones) juntas y fijadas en su lugar. La materia en estado líquido mantiene un volumen fijo, pero tiene una forma variable que se adapta a su contenedor. Sus partículas aún están juntas, pero se mueven libremente. La materia en estado gaseoso tiene tanto un volumen como una forma variables, adaptándose ambos para adaptarse a su contenedor. Sus partículas no están ni juntas ni fijadas en su lugar. La materia en estado de plasma tiene volumen y forma variables, pero además de átomos neutros, contiene una cantidad importante de iones y electrones, que pueden moverse libremente.
El término fase se usa a veces como sinónimo del estado de la materia, pero un sistema puede contener varias fases inmiscibles del mismo estado de la materia.
Los cuatro estados fundamentales
Sólido
En un sólido, las partículas constituyentes (iones, átomos o moléculas) se agrupan juntas. Las fuerzas entre las partículas son tan fuertes que las partículas no pueden moverse libremente, solo pueden vibrar. Como resultado, un sólido tiene una forma estable, definida y un volumen definido. Los sólidos solo pueden cambiar su forma por la fuerza, como cuando se rompen o cortan.
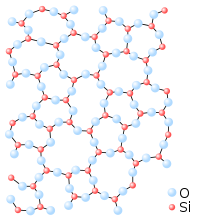
En sólidos cristalinos, las partículas (átomos, moléculas o iones) se empaquetan en un patrón repetitivo ordenado regularmente. Existen varias estructuras cristalinas diferentes, y la misma sustancia puede tener más de una estructura (o fase sólida). Por ejemplo, el hierro tiene una estructura cúbica centrada en el cuerpo a temperaturas por debajo de 912 ° C, y una estructura cúbica centrada en la cara entre 912 y 1394 ° C. El hielo tiene quince estructuras cristalinas conocidas, o quince fases sólidas, que existen a diversas temperaturas y presiones.
Los vidrios y otros sólidos amorfos no cristalinos sin orden de largo alcance no son estados de equilibrio térmico del suelo; por lo tanto, se describen a continuación como estados de la materia no clásicos.
Los sólidos pueden transformarse en líquidos fundiéndose y los líquidos pueden transformarse en sólidos por congelación. Los sólidos también pueden transformarse directamente en gases a través del proceso de sublimación, y los gases también pueden transformarse directamente en sólidos a través de la deposición.
Líquido
Un líquido es un fluido casi incompresible que se adapta a la forma de su recipiente pero retiene un volumen (casi) constante independientemente de la presión. El volumen es definitivo si la temperatura y la presión son constantes. Cuando un sólido se calienta por encima de su punto de fusión, se vuelve líquido, dado que la presión es más alta que el punto triple de la sustancia. Las fuerzas intermoleculares (o interatómicas o interiónicas) siguen siendo importantes, pero las moléculas tienen suficiente energía para moverse entre sí y la estructura es móvil. Esto significa que la forma de un líquido no es definitiva, sino que está determinada por su contenedor. El volumen suele ser mayor que el del correspondiente sólido, la excepción más conocida es el agua, H 2 O. La temperatura más alta a la que puede existir un líquido determinado es su temperatura crítica.
Gas
Un gas es un fluido compresible. No solo un gas se ajustará a la forma de su contenedor sino que también se expandirá para llenar el contenedor.
En un gas, las moléculas tienen suficiente energía cinética para que el efecto de las fuerzas intermoleculares sea pequeño (o cero para un gas ideal), y la distancia típica entre las moléculas vecinas es mucho mayor que el tamaño molecular. Un gas no tiene forma o volumen definidos, pero ocupa todo el contenedor en el que está confinado. Un líquido puede convertirse en un gas calentando a presión constante hasta el punto de ebullición, o bien reduciendo la presión a temperatura constante.
A temperaturas inferiores a su temperatura crítica, un gas también se denomina vapor y puede licuarse por compresión sola sin enfriamiento. Un vapor puede existir en equilibrio con un líquido (o sólido), en cuyo caso la presión del gas es igual a la presión de vapor del líquido (o sólido).
Un fluido supercrítico (SCF) es un gas cuya temperatura y presión están por encima de la temperatura crítica y la presión crítica respectivamente. En este estado, la distinción entre líquido y gas desaparece. Un fluido supercrítico tiene las propiedades físicas de un gas, pero su alta densidad confiere propiedades de disolvente en algunos casos, lo que conduce a aplicaciones útiles. Por ejemplo, el dióxido de carbono supercrítico se usa para extraer cafeína en la fabricación de café descafeinado.
Plasma
Como un gas, el plasma no tiene forma o volumen definidos. A diferencia de los gases, los plasmas son eléctricamente conductores, producen campos magnéticos y corrientes eléctricas, y responden fuertemente a las fuerzas electromagnéticas. Los núcleos cargados positivamente nadan en un "mar" de electrones desasociados que se mueven libremente, similar a la forma en que tales cargas existen en el metal conductor, donde este "mar" de electrones permite que la materia en el estado de plasma conduzca la electricidad.
Un gas generalmente se convierte en plasma de una de dos formas. por ejemplo, desde una enorme diferencia de voltaje entre dos puntos, o exponiéndolo a temperaturas extremadamente altas. Calentar la materia a altas temperaturas hace que los electrones abandonen los átomos, lo que resulta en la presencia de electrones libres. Esto crea un llamado plasma parcialmente ionizado. A temperaturas muy altas, como las presentes en las estrellas, se supone que esencialmente todos los electrones son "libres", y que un plasma de muy alta energía es esencialmente un núcleo desnudo nadando en un mar de electrones. Esto forma el llamado plasma completamente ionizado.
El estado del plasma a menudo se entiende mal, y aunque no existe libremente en condiciones normales en la Tierra, comúnmente se genera por rayos, chispas eléctricas, luces fluorescentes, luces de neón o en televisores de plasma. También el plasma aparece en algunos tipos de llamas, la corona del Sol y las estrellas son ejemplos de materia iluminada en el estado del plasma.
Transiciones de fase
Un estado de la materia también se caracteriza por transiciones de fase. Una transición de fase indica un cambio en la estructura y puede reconocerse por un cambio abrupto en las propiedades. Un estado distinto de la materia se puede definir como cualquier conjunto de estados distinguidos de cualquier otro conjunto de estados por una transición de fase. Se puede decir que el agua tiene varios estados sólidos distintos. La aparición de superconductividad está asociada a una transición de fase, por lo que existen estados superconductores. Del mismo modo, los estados ferromagnéticos están demarcados por transiciones de fase y tienen propiedades distintivas. Cuando el cambio de estado ocurre por etapas, los pasos intermedios se llaman mesofases. Tales fases han sido explotadas por la introducción de la tecnología de cristal líquido.
El estado o fase de un conjunto dado de materia puede cambiar dependiendo de las condiciones de presión y temperatura, pasando a otras fases a medida que estas condiciones cambian para favorecer su existencia; por ejemplo, transiciones sólidas a líquido con un aumento de la temperatura. Cerca del cero absoluto, una sustancia existe como un sólido. A medida que se agrega calor a esta sustancia se derrite en un líquido en su punto de fusión, hierve en un gas en su punto de ebullición, y si se calienta lo suficiente podría entrar en un estado de plasma en el que los electrones están tan energizados que dejan sus átomos originales.
Las formas de materia que no están compuestas por moléculas y están organizadas por diferentes fuerzas también pueden considerarse estados diferentes de la materia. Los superfluidos (como el condensado fermiónico) y el plasma de quark-gluón son ejemplos.
En una ecuación química, el estado de la materia de los productos químicos se puede mostrar como (s) para sólidos, (l) para líquidos y (g) para gases. Una solución acuosa se denota (aq). La materia en el estado de plasma rara vez se usa (si es que se usa) en ecuaciones químicas, por lo que no existe un símbolo estándar para denotarla. En las ecuaciones raras que el plasma se usa en plasma se simboliza como (p).
Estados no clásicos
Vaso
El vidrio es un material sólido no cristalino o amorfo que exhibe una transición vítrea cuando se calienta hacia el estado líquido. Los vidrios pueden estar hechos de clases de materiales bastante diferentes: redes inorgánicas (como vidrio de ventana, hecho de silicato más aditivos), aleaciones metálicas, masas fundidas iónicas, soluciones acuosas, líquidos moleculares y polímeros. Termodinámicamente, un vidrio está en un estado metaestable con respecto a su homólogo cristalino. La tasa de conversión, sin embargo, es prácticamente cero.
Cristales con cierto grado de desorden
Un cristal plástico es un sólido molecular con un orden de posición de largo alcance pero con moléculas constituyentes que retienen la libertad de rotación; en un vaso orientacional, este grado de libertad se congela en un estado desordenado y apagado.
Del mismo modo, en un cristal giratorio el desorden magnético se congela.
Estados de cristal líquido
Los estados de cristal líquido tienen propiedades intermedias entre líquidos móviles y sólidos ordenados. En general, pueden fluir como un líquido, pero exhiben un orden de largo alcance. Por ejemplo, la fase nemática consiste en moléculas de tipo varilla larga tales como para-azoxianisol, que es nemática en el rango de temperatura 118-136 ° C. En este estado, las moléculas fluyen como en un líquido, pero todas apuntan en la misma dirección (dentro de cada dominio) y no pueden girar libremente. Como un sólido cristalino, pero a diferencia de un líquido, los cristales líquidos reaccionan a la luz polarizada.
Otros tipos de cristales líquidos se describen en el artículo principal sobre estos estados. Varios tipos tienen importancia tecnológica, por ejemplo, en pantallas de cristal líquido.
Magnéticamente ordenado
Los átomos de metal de transición a menudo tienen momentos magnéticos debido al giro neto de los electrones que permanecen sin emparejar y no forman enlaces químicos. En algunos sólidos, los momentos magnéticos en átomos diferentes se ordenan y pueden formar un ferromagnet, un antiferromagnet o un ferrimagnet.
En un ferromagnet, por ejemplo, hierro sólido, el momento magnético de cada átomo se alinea en la misma dirección (dentro de un dominio magnético). Si los dominios también están alineados, el sólido es un imán permanente, que es magnético incluso en ausencia de un campo magnético externo. La magnetización desaparece cuando el imán se calienta al punto de Curie, que para el hierro es de 768 ° C.
Un antiferromagnet tiene dos redes de momentos magnéticos iguales y opuestos, que se cancelan mutuamente de modo que la magnetización neta es cero. Por ejemplo, en el óxido de níquel (II) (NiO), la mitad de los átomos de níquel tienen momentos alineados en una dirección y la mitad en la dirección opuesta.
En un ferrimagnet, las dos redes de momentos magnéticos son opuestas pero desiguales, por lo que la cancelación es incompleta y existe una magnetización neta nula. Un ejemplo es la magnetita (Fe 3 O 4 ), que contiene iones Fe y Fe con diferentes momentos magnéticos.
Un líquido de giro cuántico (QSL) es un estado desordenado en un sistema de espines cuánticos interactuantes que conserva su desorden a temperaturas muy bajas, a diferencia de otros estados desordenados. No es un líquido en el sentido físico, sino un sólido cuyo orden magnético es inherentemente desordenado. El nombre "líquido" se debe a una analogía con el trastorno molecular en un líquido convencional. Un QSL no es ni ferromagnet, donde los dominios magnéticos son paralelos, ni antiferromagnet, donde los dominios magnéticos son antiparalelos; en cambio, los dominios magnéticos están orientados aleatoriamente. Esto puede realizarse, por ejemplo, mediante momentos magnéticos geométricamente frustrados que no pueden apuntar uniformemente paralelos o antiparalelos. Cuando se enfría y se establece en un estado, el dominio debe "elegir" una orientación, pero si los posibles estados son similares en energía, uno será elegido al azar. En consecuencia, a pesar del orden fuerte de corto alcance, no hay un orden magnético de largo alcance.
Microfase separado
Los copolímeros pueden experimentar separación por microfases para formar una serie diversa de nanoestructuras periódicas, como se muestra en el ejemplo del copolímero de bloques de estireno-butadieno-estireno que se muestra a la derecha. La separación por microfases se puede entender por analogía a la separación de fases entre el aceite y el agua. Debido a la incompatibilidad química entre los bloques, los copolímeros de bloques experimentan una separación de fase similar. Sin embargo, debido a que los bloques están covalentemente unidos entre sí, no pueden desmoronarse macroscópicamente como pueden hacerlo el agua y el aceite, por lo que los bloques forman estructuras de tamaño nanométrico. Dependiendo de las longitudes relativas de cada bloque y de la topología de bloque general del polímero, se pueden obtener muchas morfologías, cada una con su propia fase de materia.
Los líquidos iónicos también muestran separación por microfases. El anión y el catión no son necesariamente compatibles y, de otro modo, desmiendrían, pero la atracción de carga eléctrica impide que se separen. Sus aniones y cationes parecen difundirse dentro de capas compartimentadas o micelas en lugar de libremente como en un líquido uniforme.
Estados de baja temperatura
Superfluido
Cerca del cero absoluto, algunos líquidos forman un segundo estado líquido que se describe como superfluido porque tiene una viscosidad nula (o fluidez infinita, es decir, fluye sin fricción). Esto fue descubierto en 1937 para helio, que forma un superfluido por debajo de la temperatura lambda de 2,17 K. En este estado, intentará "escalar" fuera de su contenedor. También tiene una conductividad térmica infinita para que no se forme un gradiente de temperatura en un superfluido. Colocar un superfluido en un contenedor giratorio dará como resultado vórtices cuantificados.
Estas propiedades se explican por la teoría de que el isótopo común helio-4 forma un condensado de Bose-Einstein (véase la siguiente sección) en el estado superfluido. Más recientemente, los superfluidos de condensado fermiónico se han formado a temperaturas incluso más bajas por el isótopo raro helio-3 y por litio-6.
Condensado de Bose-Einstein
En 1924, Albert Einstein y Satyendra Nath Bose predijeron el "condensado de Bose-Einstein" (BEC), a veces denominado el quinto estado de la materia. En un BEC, la materia deja de comportarse como partículas independientes y se colapsa en un único estado cuántico que se puede describir con una única y uniforme función de onda.
En la fase gaseosa, el condensado Bose-Einstein permaneció como una predicción teórica no verificada durante muchos años. En 1995, los grupos de investigación de Eric Cornell y Carl Wieman, de JILA en la Universidad de Colorado en Boulder, produjeron el primer condensado de ese tipo experimentalmente. Un condensado de Bose-Einstein es "más frío" que un sólido. Puede ocurrir cuando los átomos tienen niveles cuánticos muy similares (o los mismos), a temperaturas muy cercanas al cero absoluto (-273,15 ° C).
Condensado fermiónico
Un condensado fermiónico es similar al condensado de Bose-Einstein pero está compuesto de fermiones. El principio de exclusión de Pauli impide que los fermiones entren en el mismo estado cuántico, pero un par de fermiones puede comportarse como un bosón, y múltiples pares pueden entrar en el mismo estado cuántico sin restricción.
Molécula de Rydberg
Uno de los estados metaestables del plasma fuertemente no ideal es la materia de Rydberg, que se forma tras la condensación de los átomos excitados. Estos átomos también pueden convertirse en iones y electrones si alcanzan una determinada temperatura. En abril de 2009, Nature informó la creación de moléculas de Rydberg a partir de un átomo de Rydberg y un átomo de estado fundamental, lo que confirma que tal estado de la materia podría existir. El experimento se realizó usando átomos de rubidio ultrafrío.
Estado del estado cuántico
Un estado Hall cuántico da lugar a voltaje Hall cuantificado medido en la dirección perpendicular al flujo de corriente. Un estado Hall de giro cuántico es una fase teórica que puede allanar el camino para el desarrollo de dispositivos electrónicos que disipan menos energía y generan menos calor. Esta es una derivación del estado de la materia del Salón Cuántico.
Materia fotónica
La materia fotónica es un fenómeno en el que los fotones que interactúan con un gas desarrollan masa aparente y pueden interactuar entre sí, incluso formando "moléculas" fotónicas. La fuente de la masa es el gas, que es masivo. Esto está en contraste con los fotones que se mueven en el espacio vacío, que no tienen masa en reposo y no pueden interactuar.
Dropleton
Una "niebla cuántica" de electrones y agujeros que fluyen uno alrededor del otro e incluso se ondulan como un líquido, en lugar de existir como pares discretos.
Estados de alta energía
Materia degenerada
Bajo una presión extremadamente alta, como en los núcleos de estrellas muertas, la materia ordinaria experimenta una transición a una serie de estados de materia exóticos conocidos colectivamente como materia degenerada, que se apoyan principalmente en los efectos de la mecánica cuántica. En física, "degenerado" se refiere a dos estados que tienen la misma energía y son intercambiables. La materia degenerada está respaldada por el principio de exclusión de Pauli, que impide que dos partículas fermiónicas ocupen el mismo estado cuántico. A diferencia del plasma normal, el plasma degenerado se expande poco cuando se calienta, porque simplemente no quedan estados de momento. En consecuencia, las estrellas degeneradas colapsan en densidades muy altas. Las estrellas degeneradas más masivas son más pequeñas, porque la fuerza gravitacional aumenta, pero la presión no aumenta proporcionalmente.
La materia degenerada por electrones se encuentra dentro de las estrellas enanas blancas. Los electrones permanecen unidos a los átomos pero pueden transferirse a los átomos adyacentes. La materia degenerada por neutrones se encuentra en estrellas de neutrones. La gran presión gravitacional comprime los átomos tan fuertemente que los electrones se ven obligados a combinarse con los protones a través de la desintegración beta inversa, lo que resulta en una conglomeración superdensa de neutrones. Normalmente, los neutrones libres que se encuentran fuera de un núcleo atómico se descompondrán con una vida media de poco menos de 15 minutos, pero en una estrella de neutrones, la desintegración se sobrepone a la desintegración inversa. La materia degenerada en frío también está presente en planetas como Júpiter y en las enanas marrones aún más masivas, que se espera que tengan un núcleo con hidrógeno metálico. Debido a la degeneración, las enanas marrones más masivas no son significativamente más grandes. En metales,
Quark importa
En la materia fría habitual, los quarks, partículas fundamentales de materia nuclear, están confinados por la fuerza fuerte en hadrones que constan de 2-4 quarks, como protones y neutrones. Materia de Quark o materia de chromodynanamical cuántica (QCD) es un grupo de fases donde se supera la fuerza fuerte y los quarks se desconsuelven y se mueven libremente. Las fases de la materia de Quark ocurren a densidades o temperaturas extremadamente altas, y no hay maneras conocidas de producirlas en equilibrio en el laboratorio; en condiciones normales, cualquier materia de quark formada inmediatamente sufre decaimiento radioactivo.
La materia extraña es un tipo de materia quark que se sospecha que existe dentro de algunas estrellas de neutrones cerca del límite Tolman-Oppenheimer-Volkoff (aproximadamente 2-3 masas solares), aunque no hay evidencia directa de su existencia. En materia extraña, parte de la energía disponible se manifiesta como quarks extraños, un análogo más pesado del quark down común. Puede ser estable en estados de energía más bajos una vez formados, aunque esto no se conoce.
El plasma Quark-gluón es una fase de muy alta temperatura en la cual los quarks se liberan y pueden moverse independientemente, en lugar de estar perpetuamente unidos en partículas, en un mar de gluones, partículas subatómicas que transmiten la fuerza fuerte que une a los quarks. Esto es análogo a la liberación de electrones de los átomos en un plasma. Este estado es brevemente alcanzable en colisiones de iones pesados de energía extremadamente alta en aceleradores de partículas, y permite a los científicos observar las propiedades de los quarks individuales, y no solo teorizar. El plasma de Quark-gluón fue descubierto en el CERN en 2000. A diferencia del plasma, que fluye como un gas, las interacciones dentro de QGP son fuertes y fluyen como un líquido.
A altas densidades pero a temperaturas relativamente bajas, los quarks se teorizan para formar un líquido de quark cuya naturaleza es actualmente desconocida. Forma una clara fase de color-sabor bloqueado (CFL) a densidades aún mayores. Esta fase es superconductiva para la carga de color. Estas fases pueden ocurrir en estrellas de neutrones, pero actualmente son teóricas.
Condensado de vidrio de color
El condensado de vidrio de color es un tipo de materia que se teoriza que existe en los núcleos atómicos que viajan cerca de la velocidad de la luz. De acuerdo con la teoría de la relatividad de Einstein, un núcleo de alta energía parece tener una longitud contraída o comprimida a lo largo de su dirección de movimiento. Como resultado, los gluones dentro del núcleo aparecen a un observador estacionario como una "pared gluónica" que viaja cerca de la velocidad de la luz. A energías muy altas, la densidad de los gluones en esta pared aumenta considerablemente. A diferencia del plasma de quark-gluón producido en la colisión de tales paredes, el condensado de vidrio de color describe las paredes mismas, y es una propiedad intrínseca de las partículas que solo se puede observar en condiciones de alta energía como RHIC y posiblemente en el Gran Colisionador de Hadrones también.
Estados de energía muy alta
Varias teorías predicen nuevos estados de la materia a energías muy altas. Un estado desconocido ha creado la asimetría del barión en el universo, pero se sabe poco sobre él. En la teoría de cuerdas, se predice una temperatura de Hagedorn para las supercuerdas a unos 10 K, donde las supercuerdas se producen copiosamente. A temperatura de Planck (10 K), la gravedad se convierte en una fuerza significativa entre las partículas individuales. Ninguna teoría actual puede describir estos estados y no pueden ser producidos con ningún experimento previsible. Sin embargo, estos estados son importantes en cosmología porque el universo puede haber pasado a través de estos estados en el Big Bang.
La singularidad gravitacional predicha por la relatividad general para existir en el centro de un agujero negro no es una fase de la materia; no es en absoluto un objeto material (aunque la masa-energía de la materia contribuyó a su creación), sino más bien una propiedad del espacio-tiempo en un lugar. Se podría argumentar, por supuesto, que todas las partículas son propiedades del espacio-tiempo en un lugar, dejando una nota de controversia a medias sobre el tema.
Otros estados propuestos
Supersólido
Un supersólido es un material espacialmente ordenado (es decir, un sólido o cristal) con propiedades superfluidas. Similar a un superfluido, un supersólido es capaz de moverse sin fricción pero conserva una forma rígida. Aunque un supersólido es un sólido, exhibe tantas propiedades características diferentes de otros sólidos que muchos argumentan que es otro estado de la materia.
Líquido de red
En un líquido de malla, los átomos tienen una disposición aparentemente inestable, como un líquido, pero siguen siendo consistentes en el patrón general, como un sólido. Cuando se encuentran en un estado sólido normal, los átomos de la materia se alinean en un patrón de cuadrícula, de modo que el giro de cualquier electrón es el opuesto al giro de todos los electrones que lo tocan. Pero en un líquido de red de cuerdas, los átomos están dispuestos en un patrón que requiere que algunos electrones tengan vecinos con el mismo giro. Esto da lugar a propiedades curiosas, así como apoya algunas propuestas inusuales sobre las condiciones fundamentales del universo mismo.
Superglass
Un superglass es una fase de la materia caracterizada, al mismo tiempo, por superfluidez y una estructura amorfa congelada.
Materia oscura
Mientras que la materia oscura se estima que comprende el 83% de la masa de materia en el universo, la mayoría de sus propiedades siguen siendo un misterio debido al hecho de que no absorbe ni emite radiación electromagnética, y hay muchas teorías en competencia con respecto a qué materia oscura es realmente hecho de. Por lo tanto, aunque se cree que existe y comprende la gran mayoría de la materia en el universo, casi todas sus propiedades son desconocidas y una cuestión de especulación, ya que solo se ha observado a través de sus efectos gravitacionales.