Aluminio
Definición
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades generales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciación |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| nombre alternativo | aluminio (Estados Unidos, Canadá) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | plateado gris metálico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atómico estándar ( A r, estándar) | 26.981 5385 (7) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aluminio en la tabla periódica | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número atómico ( Z ) | 13 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo | grupo 13 (grupo de boro) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Período | periodo 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoría de elemento | metal posterior a la transición, a veces considerado un metaloide | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloquear | p-block | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electronica | [Ne] 3s 3p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Electrones por caparazón | 2, 8, 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase en STP | sólido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusion | 933,47 K (660,32 ° C, 1220,58 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 2743 K (2470 ° C, 4478 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad (cerca de rt ) | 2.70 g / cm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| cuando es líquido (en mp ) | 2.375 g / cm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusión | 10.71 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de vaporización | 284 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidad de calor molar | 24,20 J / (mol • K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Presión de vapor
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidación | +3 , +2, +1, -1, -2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | Escala de Pauling: 1,61 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energías de ionización |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico | empírico: 143 p. m. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 121 ± 4 p. M. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio Van der Waals | 184 p. M. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscelánea | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | centrado en la cara cúbico (fcc) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad de la varilla delgada de sonido | (laminado) 5000 m / s (a temperatura ambiente ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansión térmica | 23.1 μm / (m • K) (a 25 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 237 W / (m • K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistividad electrica | 28.2 nΩ • m (a 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenamiento magnético | paramagnético | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Susceptibilidad magnética | + 16.5 • 10 cm / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| El módulo de Young | 70 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de corte | 26 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de volumen | 76 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relación de Poisson | 0.35 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 2.75 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Vickers | 160-350 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 160-550 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Número CAS | 7429-90-5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Historia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombrando | después de la alúmina (óxido de aluminio), llamada así por el alumbre mineral | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicción | Antoine Lavoisier (1782) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Descubrimiento y primer aislamiento | Hans Christian Ørsted (1824) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombrado por | Humphry Davy (1812) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Principales isótopos de aluminio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El aluminio es notable por su baja densidad y su capacidad para resistir la corrosión a través del fenómeno de pasivación. El aluminio y sus aleaciones son vitales para la industria aeroespacial e importantes en las industrias del transporte y la construcción, como la construcción de fachadas y marcos de ventanas. Los óxidos y sulfatos son los compuestos más útiles de aluminio.
A pesar de su prevalencia en el medio ambiente, ninguna forma conocida de vida utiliza metabólicamente las sales de aluminio, pero el aluminio es bien tolerado por las plantas y los animales. Debido a la abundancia de estas sales, el potencial para un rol biológico para ellas es de continuo interés, y los estudios continúan.
Características físicas
Núcleos e isótopos
El número atómico del aluminio es 13. De los isótopos de aluminio, solo uno es estable: Al. Esto es consistente con el hecho de que el número atómico del aluminio es impar. Es el único isótopo que ha existido en la Tierra en su forma actual desde la creación del planeta. Es esencialmente el único isótopo que representa el elemento en la Tierra, lo que hace que el aluminio sea un elemento mononuclídico y prácticamente iguale su peso atómico estándar al del isótopo. Un peso atómico estándar tan bajo de aluminio tiene algunos efectos sobre las propiedades del elemento (ver a continuación).
Todos los demás isótopos son radiactivos y no podrían haber sobrevivido; el isótopo más estable de estos es Al (vida media de 720,000 años). Al se produce a partir de argón en la atmósfera por espalación causada por protones de rayos cósmicos y se usa en radiodatos. La relación de Al a Behas se ha utilizado para estudiar el transporte, la deposición, el almacenamiento de sedimentos, los tiempos de entierro y la erosión en escalas de tiempo de 10 a 10 años. La mayoría de los científicos de meteoritos creen que la energía liberada por la descomposición de Al fue responsable del derretimiento y la diferenciación de algunos asteroides después de su formación hace 4.550 millones de años.
Los restantes isótopos de aluminio, con números de masa que van de 21 a 43, tienen vidas medias muy por debajo de una hora. Se conocen tres estados metaestables, todos con vidas medias inferiores a un minuto.
Capa electrónica
Un átomo de aluminio tiene 13 electrones, dispuestos en una configuración electrónica de [Ne] 3s3p, con tres electrones más allá de una configuración de gas noble estable. En consecuencia, las tres primeras energías combinadas de ionización de aluminio son mucho más bajas que la cuarta energía de ionización sola. El aluminio puede rendir con relativa facilidad sus tres electrones más externos en muchas reacciones químicas (ver abajo). La electronegatividad del aluminio es 1.61 (escala de Pauling).
Un átomo de aluminio libre tiene un radio de 143 p. M. Con los tres electrones más externos eliminados, el radio se reduce a 39 p. M. Para un átomo de 4 coordinadas o 53.5 p. M. Para un átomo de 6 coordinadas. A temperatura y presión estándar, los átomos de aluminio (cuando no están afectados por átomos de otros elementos) forman un sistema de cristal cúbico centrado en la cara unido por enlaces metálicos proporcionados por los electrones más externos de los átomos; por lo tanto, el aluminio (en estas condiciones) es un metal. Este sistema cristalino es compartido por algunos otros metales, como el plomo y el cobre; el tamaño de una celda unitaria de aluminio es comparable al de aquellos.
Abultar
El metal de aluminio, cuando está en cantidad, es muy brillante y se asemeja a la plata porque absorbe preferentemente la radiación ultravioleta y refleja toda la luz visible para que no imparta ningún color a la luz reflejada, a diferencia del espectro de reflectancia del cobre y el oro. Otra característica importante del aluminio es su baja densidad, 2.70 g / cm. El aluminio es relativamente suave, duradero, liviano, dúctil y maleable, con una apariencia que varía desde plateado a gris opaco, dependiendo de la rugosidad de la superficie. No es magnético y no se enciende fácilmente. Una nueva película de aluminio sirve como un buen reflector (aproximadamente el 92%) de la luz visible y un excelente reflector (tanto como el 98%) de la radiación de infrarrojo medio y lejano. La resistencia a la fluencia del aluminio puro es de 7-11 MPa, mientras que las aleaciones de aluminio tienen un límite elástico de 200 MPa a 600 MPa. El aluminio tiene aproximadamente un tercio de la densidad y la rigidez del acero. Se puede mecanizar, fundir, dibujar y extruir fácilmente.
Los átomos de aluminio están dispuestos en una estructura cúbica centrada en la cara (fcc). El aluminio tiene una energía de falla de apilamiento de aproximadamente 200 mJ / m.
El aluminio es un buen conductor térmico y eléctrico, tiene un 59% de conductividad de cobre, tanto térmico como eléctrico, mientras que solo tiene un 30% de densidad de cobre. El aluminio es capaz de superconductividad, con una temperatura crítica superconductora de 1.2 kelvin y un campo magnético crítico de aproximadamente 100 gauss (10 militeslas). El aluminio es el material más común para la fabricación de qubits superconductores.
Química
La resistencia a la corrosión puede ser excelente porque se forma una delgada capa superficial de óxido de aluminio cuando el metal desnudo se expone al aire, lo que impide una mayor oxidación, en un proceso denominado pasivación. Las aleaciones de aluminio más fuertes son menos resistentes a la corrosión debido a las reacciones galvánicas con cobre aleado. Esta resistencia a la corrosión se reduce en gran medida por sales acuosas, particularmente en presencia de metales diferentes.
En soluciones altamente ácidas, el aluminio reacciona con el agua para formar hidrógeno, y en las altamente alcalinas para formar aluminatos, la pasivación protectora bajo estas condiciones es insignificante. Principalmente porque está corroído por cloruros disueltos, como el cloruro de sodio común, las tuberías domésticas nunca están hechas de aluminio.
Sin embargo, debido a su resistencia general a la corrosión, el aluminio es uno de los pocos metales que retiene la reflectancia plateada en forma de polvo fino, por lo que es un componente importante de las pinturas de color plateado. El acabado de espejo de aluminio tiene la mayor reflectancia de cualquier metal en las regiones de 200-400 nm (UV) y de 3.000-10.000 nm (IR lejano); en el rango visible de 400-700 nm, está ligeramente superado por el estaño y la plata, y en los 700-3000 nm (cerca del infrarrojo) por la plata, el oro y el cobre.
El aluminio es oxidado por el agua a temperaturas inferiores a 280 ° C para producir hidrógeno, hidróxido de aluminio y calor:
- 2 Al + 6 H 2 O → 2 Al (OH) 3 + 3 H 2
Esta conversión es de interés para la producción de hidrógeno. Sin embargo, la aplicación comercial de este hecho presenta dificultades para eludir la capa de óxido de pasivación, que inhibe la reacción, y para almacenar la energía requerida para regenerar el metal de aluminio.
Compuestos inorgánicos
La gran mayoría de los compuestos, incluidos todos los minerales que contienen Al y todos los compuestos de aluminio comercialmente significativos, presentan aluminio en el estado de oxidación 3+. El número de coordinación de tales compuestos varía, pero generalmente Al es de seis coordenadas o tetracoordinado. Casi todos los compuestos de aluminio (III) son incoloros.
Los cuatro trihaluros son bien conocidos. A diferencia de las estructuras de los tres trihaluros más pesados, el fluoruro de aluminio (AlF 3 ) presenta seis coordenadas Al. El entorno de coordinación octaédrica para AlF 3 está relacionado con la compacidad del ion fluoruro, seis de los cuales pueden caber alrededor del pequeño centro de Al. AlF 3 sublimes (con grietas) a 1.291 ° C (2.356 ° F). Con haluros más pesados, los números de coordinación son más bajos. Los otros trihaluros son diméricos o poliméricos con centros tetraédricos de Al. Estos materiales se preparan tratando metal de aluminio con halógeno, aunque existen otros métodos. La acidificación de los óxidos o hidróxidos proporciona hidratos. En solución acuosa, los haluros a menudo forman mezclas, que generalmente contienen centros de Al de seis coordenadas que presentan ligandos tanto de haluro como de aquo. Cuando el aluminio y el flúor están juntos en solución acuosa, forman fácilmente iones complejos como [AlF (H
2 O)
5 ]2+
, AlF
3 (H
2 O)
3 y [AlF
6 ]3-
. En el caso del cloruro, se forman agrupaciones de polialuminio tales como [Al 13 O 4 (OH) 24 (H 2 O) 12 ].
2 O)
5 ]2+
, AlF
3 (H
2 O)
3 y [AlF
6 ]3-
. En el caso del cloruro, se forman agrupaciones de polialuminio tales como [Al 13 O 4 (OH) 24 (H 2 O) 12 ].
El aluminio forma un óxido estable con la fórmula química Al 2 O 3. Se puede encontrar en la naturaleza en el corindón mineral. El óxido de aluminio también se llama comúnmente alúmina. El zafiro y el rubí son corindón impuro contaminado con trazas de otros metales. Los dos hidróxidos de óxido, AlO (OH), son bohemita y diaspora. Hay tres trihidróxidos: bayerita, gibbsita y nordstrandita, que difieren en su estructura cristalina (polimorfos). La mayoría se producen a partir de minerales mediante una variedad de procesos húmedos que usan ácido y base. Calentar los hidróxidos conduce a la formación de corindón. Estos materiales son de importancia central para la producción de aluminio y son extremadamente útiles.
El carburo de aluminio (Al 4 C 3 ) se produce calentando una mezcla de los elementos por encima de 1,000 ° C (1,832 ° F). Los cristales de color amarillo pálido consisten en centros tetraédricos de aluminio. Reacciona con agua o ácidos diluidos para dar metano. El acetiluro, Al 2 (C 2 ) 3 , se hace mediante el paso de acetileno a través de aluminio calentado.
El nitruro de aluminio (AlN) es el único nitruro conocido para el aluminio. A diferencia de los óxidos, presenta centros tetraédricos de Al. Se puede hacer a partir de los elementos a 800 ° C (1,472 ° F). Es material estable al aire con una conductividad térmica útil alta. El fosfuro de aluminio (AlP) se fabrica de manera similar; se hidroliza para dar fosfina:
- AlP + 3 H 2 O → Al (OH) 3 + PH 3
Estados de oxidación más raros
Aunque la gran mayoría de los compuestos de aluminio presentan centros Al, se conocen compuestos con estados de oxidación más bajos y en algún momento significativos como precursores de la especie Al.
Aluminio (I)
AlF, AlCl y AlBr existen en la fase gaseosa cuando el trihaluro se calienta con aluminio. La composición AlI es inestable a temperatura ambiente, convirtiéndose en triyoduro:
Un derivado estable de monoioduro de aluminio es el aducto cíclico formado con trietilamina, Al 4 I 4 (NEt 3 ) 4 . También de interés teórico pero solo de existencia fugaz se encuentran Al 2 O y Al 2 S. Al 2 O se produce calentando el óxido normal, Al 2 O 3 , con silicio a 1.800 ° C (3.272 ° F) en vacío. Tales materiales rápidamente desproporcionan a los materiales de partida.
Aluminio (II)
Los compuestos de Al (II) muy simples se invocan u observan en las reacciones de Al metal con oxidantes. Por ejemplo, el monóxido de aluminio, AlO, se ha detectado en la fase gaseosa después de la explosión y en los espectros de absorción estelar. Se investigan más a fondo los compuestos de fórmula R 4 Al 2 que contienen un enlace Al-Al y donde R es un ligando orgánico grande.
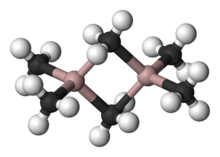
Existe una variedad de compuestos de fórmula empírica AlR 3 y AlR 1.5 Cl 1.5 . Estas especies suelen presentar centros Al tetraédricos formados por dimerización con algunos puentes R o Cl entre ambos átomos de Al, por ejemplo, "trimetilaluminio" tiene la fórmula Al 2 (CH 3 ) 6 (ver figura). Con grandes grupos orgánicos, los compuestos de triorganoaluminio existen como monómeros de tres coordenadas, como el triisobutilaluminio. Tales compuestos son ampliamente utilizados en la química industrial, a pesar de que a menudo son altamente pirofóricos. Existen pocos análogos entre los compuestos de organoaluminio y organoboro que no sean grandes grupos orgánicos.
El hidruro de aluminio de importancia industrial es el hidruro de litio y aluminio (LiAlH 4 ), que se usa como agente reductor en la química orgánica. Se puede producir a partir de hidruro de litio y tricloruro de aluminio:
- 4 LiH + AlCl 3 → LiAlH 4 + 3 LiCl
Varios derivados útiles de LiAlH 4 se conocen, por ejemplo bis dihydridoaluminate (2-metoxietoxi) sodio. El hidruro más simple, hidruro de aluminio o alane, sigue siendo una curiosidad de laboratorio. Es un polímero con la fórmula (ALH 3 ) n , en contraste con el correspondiente hidruro de boro que es un dímero con la fórmula (BH 3 ) 2 .
Ocurrencia natural
En el espacio
La abundancia de partículas de aluminio en el Sistema Solar es de 3.15 ppm (partes por millón). Es el duodécimo más abundante de todos los elementos y el tercero más abundante entre los elementos que tienen números atómicos impares, después del hidrógeno y el nitrógeno. El único isótopo estable del aluminio, Al, es el décimo octavo núcleo más abundante en el Universo. Se crea casi en su totalidad después de la fusión del carbono en estrellas masivas que luego se convertirán en supernovas de Tipo II: esta fusión crea Mg, que al capturar protones y neutrones libres se convierte en aluminio. Algunas cantidades más pequeñas de Al se crean en capas de combustión de hidrógeno de estrellas evolucionadas, donde el Mg puede capturar protones libres. Esencialmente todo el aluminio ahora en existencia es Al; Al estuvo presente en el Sistema Solar temprano, pero actualmente está extinto. Sin embargo,
En la tierra
En general, la Tierra es aproximadamente 1,59% de aluminio en masa (séptimo en abundancia en masa). El aluminio se produce en mayor proporción en la Tierra que en el Universo porque el aluminio forma fácilmente el óxido y se une a las rocas y el aluminio se queda en la corteza terrestre mientras que los metales menos reactivos se hunden en el núcleo. En la corteza terrestre, el aluminio es el elemento metálico más abundante (8,3% en masa) y el tercero más abundante de todos los elementos (después del oxígeno y el silicio). Una gran cantidad de silicatos en la corteza terrestre contienen aluminio. En contraste, el manto de la Tierra es solo 2.38% de aluminio en masa.
Debido a su fuerte afinidad por el oxígeno, el aluminio casi nunca se encuentra en el estado elemental; en cambio, se encuentra en óxidos o silicatos. Los feldespatos, el grupo más común de minerales en la corteza terrestre, son aluminosilicatos. El aluminio también se produce en los minerales berilo, criolita, granate, espinela y turquesa. Las impurezas en Al 2 O 3 , como el cromo y el hierro, producen las piedras preciosas rubí y zafiro, respectivamente. El metal de aluminio nativo solo se puede encontrar como una fase menor en ambientes de fugacidad baja en oxígeno, como el interior de ciertos volcanes. Se ha informado sobre el aluminio nativo en filtraciones frías en la vertiente continental nororiental del Mar del Sur de China. Es posible que estos depósitos sean el resultado de la reducción bacteriana de tetrahidroxoaluminato de Al (OH) 4.
Aunque el aluminio es un elemento común y generalizado, no todos los minerales de aluminio son fuentes económicamente viables del metal. Casi todo el aluminio metálico se produce a partir de la bauxita de mineral (AlO x (OH) 3-2 x ). La bauxita se produce como un producto de intemperie de bajo contenido de hierro y roca madre de sílice en condiciones climáticas tropicales. En 2017, la mayoría de la bauxita se extrajo en Australia, China, Guinea e India.
Historia
La historia del aluminio ha sido moldeada por el uso de alumbre. El primer registro escrito de alumbre, hecho por el historiador griego Herodoto, se remonta al siglo V a. Se sabe que los antiguos usaron alumbre como tintóreos y para la defensa de la ciudad. Después de las Cruzadas, el alumbre, un buen elemento indispensable en la industria textil europea, fue objeto de comercio internacional; fue importado a Europa desde el Mediterráneo oriental hasta mediados del siglo XV.
La naturaleza del alumbre sigue siendo desconocida. Alrededor de 1530, el médico suizo Paracelso sugirió que el alumbre era una sal de una tierra de alumbre. En 1595, el médico y químico alemán Andreas Libavius lo confirmó experimentalmente; En 1722, el químico alemán Friedrich Hoffmann anunció su creencia de que la base del alumbre era una tierra distinta. En 1754, el químico alemán Andreas Sigismund Marggraf sintetizó alúmina hirviendo arcilla en ácido sulfúrico y posteriormente añadiendo potasa.
Los intentos de producir metal de aluminio datan de 1760. El primer intento exitoso, sin embargo, fue completado en 1824 por el físico y químico danés Hans Christian Ørsted. Reaccionó cloruro de aluminio anhidro con amalgama de potasio, produciendo un trozo de metal que se parece al estaño. Presentó sus resultados y demostró una muestra del nuevo metal en 1825. En 1827, el químico alemán Friedrich Wöhler repitió los experimentos de Ørsted pero no identificó ningún aluminio. (La razón de esta inconsistencia solo se descubrió en 1921.) Realizó un experimento similar en 1827 al mezclar cloruro de aluminio anhidro con potasio y produjo un polvo de aluminio. En 1845, pudo producir pequeñas piezas de metal y describió algunas propiedades físicas de este metal. Por muchos años después, Wöhler fue acreditado como el descubridor de aluminio después del éxito y los detalles descriptivos de su experimento de 1845. Como el método de Wöhler no podía producir grandes cantidades de aluminio, el metal seguía siendo raro; Su costo excedió el del oro.
El químico francés Henri Etienne Sainte-Claire Deville anunció un método industrial de producción de aluminio en 1854 en la Academia de Ciencias de París. El tricloruro de aluminio se podía reducir con sodio, que era más conveniente y menos costoso que el potasio, que Wöhler había usado. En 1856, Deville junto con sus compañeros establecieron la primera producción industrial de aluminio del mundo. De 1855 a 1859, el precio del aluminio cayó en un orden de magnitud, de US $ 500 a $ 40 por libra. Incluso entonces, el aluminio aún no era de gran pureza y el aluminio producido difería en las propiedades por muestra.
El primer método industrial de producción a gran escala fue desarrollado independientemente en 1886 por el ingeniero francés Paul Héroult y el ingeniero estadounidense Charles Martin Hall; ahora se conoce como el proceso Hall-Héroult. El proceso de Hall-Héroult convierte la alúmina en metal. El químico austríaco Carl Joseph Bayer descubrió una forma de purificar la bauxita para producir alúmina, ahora conocida como el proceso de Bayer, en 1889. La producción moderna del metal de aluminio se basa en los procesos de Bayer y Hall-Héroult. El proceso de Hall-Héroult fue mejorado en 1920 por un equipo dirigido por el químico sueco Carl Wilhelm Söderberg; esta mejora incrementó en gran medida la producción mundial de aluminio.
Los precios del aluminio cayeron y el aluminio se utilizó ampliamente en joyería, artículos de uso cotidiano, marcos de gafas, instrumentos ópticos, vajillas y papel de aluminio en la década de 1890 y principios del siglo XX. La capacidad del aluminio de formar aleaciones duras pero ligeras con otros metales proporcionó muchos usos al metal en ese momento. Durante la Primera Guerra Mundial, los principales gobiernos exigieron grandes envíos de aluminio para armaduras ligeras y fuertes.
A mediados del siglo XX, el aluminio se había convertido en parte de la vida cotidiana, convirtiéndose también en un componente esencial de los artículos para el hogar. Durante la mitad del siglo 20, el aluminio surgió como un material de ingeniería civil, con edificios que utilizan tanto la construcción básica y el interior, y avanzó su uso en la ingeniería militar, tanto para aviones y motores de vehículos blindados. El primer satélite artificial de la Tierra, lanzado en 1957, consistía en dos semiesferas de aluminio separadas unidas entre sí y todos los vehículos espaciales posteriores se han fabricado en aluminio. La lata de aluminio se inventó en 1956 y se utilizó como depósito de bebidas en 1958.
A lo largo del siglo XX, la producción de aluminio aumentó rápidamente: mientras que la producción mundial de aluminio en 1900 fue de 6.800 toneladas métricas, la producción anual superó por primera vez las 100.000 toneladas métricas en 1916; 1,000,000 de toneladas en 1941; 10,000,000 de toneladas en 1971. En la década de 1970, la mayor demanda de aluminio lo convirtió en un producto de intercambio; entró en la Bolsa de Metales de Londres, la bolsa de metal industrial más antigua del mundo, en 1978. La producción continuó creciendo: la producción anual de aluminio superó las 50,000,000 toneladas métricas en 2013.
El precio real del aluminio disminuyó de $ 14,000 por tonelada métrica en 1900 a $ 2,340 en 1948 (en dólares de los Estados Unidos en 1998). Los costos de extracción y procesamiento se redujeron sobre el progreso tecnológico y la escala de las economías. Sin embargo, la necesidad de explotar los depósitos de calidad inferior y de menor calidad y el uso de costos de insumos cada vez más rápidos (sobre todo, energía) aumentaron el costo neto del aluminio; el precio real comenzó a crecer en la década de 1970 con el aumento del costo de la energía. La producción se trasladó desde los países industrializados a países donde la producción era más barata. Los costos de producción a fines del siglo XX cambiaron debido a los avances en la tecnología, los bajos precios de la energía, los tipos de cambio del dólar de los Estados Unidos y los precios de la alúmina. La cuota combinada de los países BRIC creció en la primera década del siglo XXI del 32,6% al 56. 5% en producción primaria y 21.4% a 47.8% en consumo primario. China está acumulando una porción especialmente grande de la producción mundial gracias a la abundancia de recursos, energía barata y estímulos gubernamentales; también aumentó su participación de consumo del 2% en 1972 al 40% en 2010. En los Estados Unidos, Europa Occidental y Japón, la mayor parte del aluminio se consumió en transporte, ingeniería, construcción y embalaje.
Etimología
El aluminio lleva el nombre de la alúmina u óxido de aluminio en la nomenclatura moderna. La palabra "alúmina" proviene del "alumbre", el mineral del que se obtuvo. La palabra "alumbre" proviene de alumen , una palabra latina que significa "sal amarga". La palabra alumen proviene de la raíz proto-indoeuropea * alu- que significa "amargo" o "cerveza".
El químico británico Humphry Davy, que realizó una serie de experimentos destinados a sintetizar el metal, se acredita como la persona que nombró al aluminio. En 1808, sugirió que el metal se llamara alumium . Esta sugerencia fue criticada por los químicos contemporáneos de Francia, Alemania y Suecia, que insistieron en que el metal debe ser nombrado para el óxido, la alúmina, de la que sería aislado. En 1812, Davy eligió el aluminio , produciendo así el nombre moderno. Sin embargo, se deletrea y se pronuncia de manera diferente fuera de América del Norte: el aluminio está en uso en los EE. UU. Y Canadá, mientras que el aluminio está en uso en otros lugares.
Ortografía
El sufijo -ium siguió el precedente establecido en otros elementos recientemente descubiertos de la época: potasio, sodio, magnesio, calcio y estroncio (todos los cuales se aisló Davy). Sin embargo, los nombres de elementos que terminan en -um no eran desconocidos en ese momento; por ejemplo, platino (conocido por los europeos desde el siglo XVI), molibdeno (descubierto en 1778) y tantalio (descubierto en 1802). El sufijo -um es consistente con la alúmina ortográfica universal para el óxido (en oposición a la aluminia); compárese con lanthana, el óxido de lantano, y la magnesia, la ceria y la toria, los óxidos de magnesio, cerio y torio, respectivamente.
En 1812, el científico británico Thomas Young escribió una reseña anónima del libro de Davy, en la que objetó el aluminio y propuso el nombre de aluminio : "así que nos tomaremos la libertad de escribir la palabra, con preferencia al aluminio, que tiene un aspecto menos clásico". sonar." Este nombre sí se entendió: mientras que la ortografía -um se usaba ocasionalmente en Gran Bretaña, el lenguaje científico estadounidense usó -ium desde el principio. La mayoría de los científicos utilizaron -ium en todo el mundo en el siglo XIX; sigue siendo el estándar en la mayoría de los otros idiomas. En 1828, el lexicógrafo estadounidense Noah Webster utilizó exclusivamente la ortografía de aluminio en su diccionario estadounidense de la lengua inglesa.. En la década de 1830, la ortografía -um comenzó a ganar popularidad en los Estados Unidos; en la década de 1860, se había convertido en la ortografía más común allí fuera de la ciencia. En 1892, Hall utilizó la ortografía -um en su prospecto de publicidad para su nuevo método electrolítico de producción del metal, a pesar de su uso constante de la ortografía -ium en todas las patentes que presentó entre 1886 y 1903. Posteriormente se sugirió que se trataba de una error tipográfico en lugar de intencionado. Hacia 1890, ambos deletreos habían sido comunes en los EE. UU. En general, la ortografía del -ium siendo levemente más común; hacia 1895, la situación se había revertido; para 1900, el aluminio había sido dos veces más común que el aluminio ; durante la década siguiente, el -umla ortografía domina el uso estadounidense. En 1925, la American Chemical Society adoptó esta ortografía.
La Unión Internacional de Química Pura y Aplicada (IUPAC) adoptó el aluminio como el nombre internacional estándar para el elemento en 1990. En 1993, reconocieron al aluminio como una variante aceptable; lo mismo es cierto para la edición 2005 más reciente de la nomenclatura IUPAC de química inorgánica. Las publicaciones oficiales de la IUPAC usan la ortografía del -ium como primaria, pero enumeran ambas cuando corresponda. La Wikipedia en inglés sigue este estándar adoptando la ortografía "aluminio" como la única ortografía en artículos relacionados con la química.
Producción y refinamiento
La producción de aluminio consume mucha energía, por lo que los productores tienden a ubicar fundiciones en lugares donde la energía eléctrica es abundante y económica. A partir de 2012, las fundiciones de aluminio más grandes del mundo se encuentran en China, Rusia, Bahrein, Emiratos Árabes Unidos y Sudáfrica.
En 2016, China fue el principal productor de aluminio con una participación mundial del cincuenta y cinco por ciento; los siguientes países productores más grandes fueron Rusia, Canadá, India y los Emiratos Árabes Unidos.
Según el informe de Metal Stocks in Society del Panel de Recursos Internacionales, el stock per cápita mundial de aluminio en uso en la sociedad (es decir, en automóviles, edificios, productos electrónicos, etc.) es de 80 kg (180 lb). Gran parte de esto se encuentra en países más desarrollados (350-500 kg (770-1.100 lb) per cápita) en lugar de países menos desarrollados (35 kg (77 lb) per cápita).
Proceso de Bayer
La bauxita se convierte en óxido de aluminio por el proceso de Bayer. La bauxita se mezcla para obtener una composición uniforme y se muele. La suspensión espesa resultante se mezcla con una solución caliente de hidróxido de sodio; la mezcla luego se trata en un recipiente digestor a una presión muy superior a la atmosférica, disolviendo el hidróxido de aluminio en bauxita mientras se convierten las impurezas en compuestos relativamente insolubles:
- Al (OH) 3 + Na + OH → Na + [Al (OH) 4 ]
Después de esta reacción, la suspensión se encuentra a una temperatura superior a su punto de ebullición atmosférico. Se enfría al eliminar el vapor a medida que se reduce la presión. El residuo de bauxita se separa de la solución y se descarta. La solución, libre de sólidos, se siembra con pequeños cristales de hidróxido de aluminio; esto causa la descomposición de los iones de [Al (OH) 4 ] en hidróxido de aluminio. Después de que ha precipitado aproximadamente la mitad del aluminio, la mezcla se envía a los clasificadores. Se recogen pequeños cristales de hidróxido de aluminio para servir como agentes de siembra; las partículas gruesas se reducen a óxido de aluminio; el exceso de solución se elimina por evaporación, (si es necesario) se purifica y se recicla.
Proceso Hall-Héroult
La conversión de alúmina en aluminio metálico se logra mediante el proceso Hall-Héroult. En este proceso que consume mucha energía, se electroliza una solución de alúmina en una mezcla fundida (950 y 980 ° C (1,740 y 1,800 ° F) de criolita (Na 3 AlF 6 ) con fluoruro de calcio para producir aluminio metálico. El metal líquido de aluminio se hunde en el fondo de la solución y se desprende, y por lo general se vierte en bloques grandes llamados palanquillas de aluminio para su posterior procesamiento.
Los ánodos de la celda de electrólisis están hechos de carbono, el material más resistente contra la corrosión por flúor, y se hornean en el proceso o se hornean previamente. Los primeros, también llamados ánodos Söderberg, son menos eficientes en términos de energía y los vapores liberados durante la cocción son costosos de recolectar, razón por la cual están siendo reemplazados por ánodos precocidos aunque ahorran energía, energía y mano de obra para precalentar los cátodos. El carbono para los ánodos debe ser preferiblemente puro para que ni el aluminio ni el electrolito estén contaminados con ceniza. A pesar de la resistividad del carbono contra la corrosión, todavía se consume a razón de 0.4-0.5 kg por cada kilogramo de aluminio producido. Los cátodos están hechos de antracita; no se requiere alta pureza para ellos porque las impurezas se filtran muy lentamente. El cátodo se consume a una tasa de 0.02-0. 04 kg por cada kilogramo de aluminio producido. Una célula generalmente termina después de 2-6 años después de una falla del cátodo.
El proceso de Hall-Heroult produce aluminio con una pureza superior al 99%. Se puede realizar una purificación adicional mediante el proceso de Hoopes. Este proceso involucra la electrólisis de aluminio fundido con un electrolito de fluoruro de sodio, bario y aluminio. El aluminio resultante tiene una pureza del 99,99%.
La energía eléctrica representa entre el 20 y el 40% del costo de producción de aluminio, dependiendo de la ubicación de la fundición. La producción de aluminio consume aproximadamente el 5% de la electricidad generada en los Estados Unidos. Debido a esto, se han investigado alternativas al proceso de Hall-Héroult, pero ninguna ha resultado económicamente factible.
Reciclaje
La recuperación del metal a través del reciclaje se ha convertido en una tarea importante de la industria del aluminio. El reciclaje fue una actividad de bajo perfil hasta fines de la década de 1960, cuando el uso creciente de latas de bebidas de aluminio lo hizo público. Reciclar implica derretir la chatarra, un proceso que requiere solo el 5% de la energía utilizada para producir aluminio a partir del mineral, aunque una parte significativa (hasta 15% del material de entrada) se pierde como escoria (óxido similar a la ceniza). Un fusor de apilamiento de aluminio produce significativamente menos escoria, con valores informados por debajo del 1%.
La escoria blanca de la producción primaria de aluminio y de las operaciones secundarias de reciclaje todavía contiene cantidades útiles de aluminio que pueden extraerse industrialmente. El proceso produce palanquillas de aluminio, junto con un material de desecho altamente complejo. Este desperdicio es difícil de manejar. Reacciona con el agua, liberando una mezcla de gases (que incluye, entre otros, hidrógeno, acetileno y amoníaco), que se enciende espontáneamente al contacto con el aire; el contacto con aire húmedo da como resultado la liberación de grandes cantidades de gas de amoníaco. A pesar de estas dificultades, el desecho se utiliza como relleno en asfalto y hormigón.
Aplicaciones
Metal
El aluminio es el metal no ferroso más utilizado. La producción mundial de aluminio en 2016 fue de 58.8 millones de toneladas métricas. Excedió el de cualquier otro metal excepto el hierro (1,231 millones de toneladas métricas).
El aluminio casi siempre está aleado, lo que mejora notablemente sus propiedades mecánicas, especialmente cuando está templado. Por ejemplo, las latas de aluminio y las latas de bebidas comunes son aleaciones de 92% a 99% de aluminio. Los principales agentes de aleación son cobre, zinc, magnesio, manganeso y silicio (por ejemplo, duraluminio) con los niveles de otros metales en un pequeño porcentaje en peso.
Los principales usos del aluminio metálico se encuentran en:
- Transporte (automóviles, aviones, camiones, vagones de ferrocarril, embarcaciones marinas, bicicletas, naves espaciales, etc.). El aluminio se utiliza debido a su baja densidad;
- Embalaje (latas, papel de aluminio, marco, etc.). El aluminio se usa porque no es tóxico, no es adsorbente y es a prueba de astillas;
- Construcción y construcción (ventanas, puertas, revestimiento, alambre para construcción, revestimiento, techado, etc.). Como el acero es más barato, el aluminio se usa cuando la ligereza, la resistencia a la corrosión o las características de ingeniería son importantes;
- Usos relacionados con la electricidad (aleaciones de conductores, motores y generadores, transformadores, condensadores, etc.). El aluminio se utiliza porque es relativamente barato, altamente conductivo, tiene una resistencia mecánica adecuada y baja densidad, y resiste la corrosión;
- Una amplia gama de artículos para el hogar, desde utensilios de cocina hasta muebles. Baja densidad, buena apariencia, facilidad de fabricación y durabilidad son los factores clave del uso de aluminio;
- Maquinaria y equipo (equipos de procesamiento, tuberías, herramientas). El aluminio se utiliza debido a su resistencia a la corrosión, no piroforicidad y resistencia mecánica.
- Las monedas en moneda usan aluminio en denominaciones pequeñas.
Compuestos
La gran mayoría (alrededor del 90%) de óxido de aluminio se convierte en aluminio metálico. Al ser un material muy duro (dureza Mohs 9), la alúmina se usa ampliamente como abrasivo, ya que es extraordinariamente inerte desde el punto de vista químico y es útil en entornos altamente reactivos, como las lámparas de sodio de alta presión. El óxido de aluminio se usa comúnmente como catalizador para procesos industriales; por ejemplo, el proceso Claus para convertir sulfuro de hidrógeno en azufre en refinerías y para alquilar aminas. Muchos catalizadores industriales están soportados por la alúmina, lo que significa que el costoso material catalizador se dispersa sobre una superficie de la alúmina inerte. Otro uso principal es como agente de secado o absorbente.
Varios sulfatos de aluminio tienen aplicaciones industriales y comerciales. El sulfato de aluminio (en su forma de hidrato) se produce en la escala anual de varios millones de toneladas métricas. Aproximadamente dos tercios se consumen en el tratamiento del agua. La siguiente aplicación principal es en la fabricación de papel. También se usa como mordiente en el teñido, en el decapado de semillas, en la desodorización de aceites minerales, en el curtido del cuero y en la producción de otros compuestos de aluminio. Dos tipos de alumbre, alumbre de amonio y alumbre de potasio, se utilizaron anteriormente como mordientes y curtido de cuero, pero su uso ha disminuido significativamente después de la disponibilidad de sulfato de aluminio de alta pureza. El cloruro de aluminio anhidro se utiliza como catalizador en las industrias químicas y petroquímicas, la industria del tinte y en la síntesis de diversos compuestos inorgánicos y orgánicos. Los hidroxicloruros de aluminio se usan para purificar agua, en la industria del papel y como antitranspirantes. El aluminato de sodio se usa en el tratamiento del agua y como acelerador de la solidificación del cemento.
Muchos compuestos de aluminio tienen aplicaciones de nicho, por ejemplo:
- El acetato de aluminio en solución se usa como astringente.
- El fosfato de aluminio se utiliza en la fabricación de productos de vidrio, cerámica, pulpa y papel, cosméticos, pinturas, barnices y cemento dental.
- El hidróxido de aluminio se usa como un antiácido y mordiente; se usa también en la purificación de agua, la fabricación de vidrio y cerámica, y en las telas impermeabilizantes.
- El hidruro de litio y aluminio es un potente agente reductor utilizado en química orgánica.
- Los organoaluminios se usan como ácidos de Lewis y cocatalizadores.
- El metilaluminoxano es un cocatalizador de la polimerización de olefinas Ziegler-Natta para producir polímeros de vinilo como el polieteno.
- Los iones de aluminio acuosos (como el sulfato de aluminio acuoso) se usan para tratar los parásitos de peces como Gyrodactylus salaris .
- En muchas vacunas, ciertas sales de aluminio sirven como un adyuvante inmune (refuerzo de la respuesta inmune) para permitir que la proteína en la vacuna alcance una potencia suficiente como estimulante inmunológico.
Biología
A pesar de su ocurrencia generalizada en la corteza terrestre, el aluminio no tiene una función conocida en biología. Las sales de aluminio son notablemente no tóxico, sulfato de aluminio que tiene un LD
50 de 6.207 mg / kg (oral, ratón), que corresponde a 500 gramos durante 80 kg (180 lb) persona.
50 de 6.207 mg / kg (oral, ratón), que corresponde a 500 gramos durante 80 kg (180 lb) persona.
Toxicidad
En la mayoría de las personas, el aluminio no es tan tóxico como los metales pesados. El Departamento de Salud y Servicios Humanos de los Estados Unidos clasifica al aluminio como no carcinógeno. Hay poca evidencia de que la exposición normal al aluminio presente un riesgo para un adulto sano, y no hay evidencia de toxicidad si se consume en cantidades no superiores a 40 mg / día por kg de masa corporal. La mayor parte del aluminio consumido dejará el cuerpo en heces; la pequeña parte de ella que ingresa al cuerpo, se excretará a través de la orina. El aluminio que permanece en el cuerpo se acumula, sobre todo, hueso; y, aparte de eso, en cerebro, hígado y riñón. El metal de aluminio no puede pasar la barrera hematoencefálica y los filtros naturales antes que el cerebro, pero algunos compuestos, como el flúor, sí pueden hacerlo.
Efectos
El aluminio, aunque raramente, puede causar osteomalacia resistente a la vitamina D, anemia microcítica resistente a la eritropoyetina y alteraciones del sistema nervioso central. Las personas con insuficiencia renal corren un riesgo especial. La ingestión crónica de silicatos de aluminio hidratados (por exceso de control de la acidez gástrica) puede ocasionar que el aluminio se una al contenido intestinal y aumente la eliminación de otros metales, como hierro o zinc; dosis suficientemente altas (> 50 g / día) pueden causar la anemia. Dado que el aluminio se excreta por los riñones, su función puede verse afectada por las cantidades tóxicas de aluminio.
Un accidente en Inglaterra reveló que las cantidades milimolares de aluminio en el agua potable causan déficits cognitivos significativos. Las sales de aluminio ingeridas por vía oral pueden depositarse en el cerebro. Hay investigaciones sobre la correlación entre los trastornos neurológicos, incluida la enfermedad de Alzheimer y los niveles de aluminio, pero hasta ahora no ha sido concluyente.
El aluminio aumenta la expresión génica relacionada con el estrógeno en células de cáncer de mama humano cultivadas en el laboratorio. En dosis muy altas, el aluminio se asocia con una función alterada de la barrera hematoencefálica. Un pequeño porcentaje de personas tiene alergias de contacto al aluminio y experimenta erupciones rojas con picazón, dolor de cabeza, dolor muscular, dolor en las articulaciones, memoria deficiente, insomnio, depresión, asma, síndrome del intestino irritable u otros síntomas al contacto con productos que contienen aluminio.
La exposición a vapores de soldadura de aluminio o aluminio en polvo puede causar fibrosis pulmonar. El polvo de aluminio fino puede encenderse o explotar, presentando otro peligro en el lugar de trabajo.
Rutas de exposición
La comida es la principal fuente de aluminio. El agua potable contiene más aluminio que alimentos sólidos; sin embargo, el aluminio en los alimentos puede absorberse más que el aluminio del agua. Las principales fuentes de exposición oral humana al aluminio incluyen alimentos (debido a su uso en aditivos alimentarios, envases de alimentos y bebidas y utensilios de cocina), agua potable (debido a su uso en el tratamiento de aguas municipales) y medicamentos que contienen aluminio (particularmente antiácidos) / antiulcer y formulaciones de aspirina tamponada). La exposición dietética en los europeos promedia a 0.2-1.5 mg / kg / semana pero puede ser tan alta como 2.3 mg / kg / semana. Los niveles de exposición más altos de aluminio se limitan principalmente a mineros, trabajadores de producción de aluminio y pacientes de diálisis.
El consumo excesivo de antiácidos, antitranspirantes, vacunas y cosméticos proporciona niveles de exposición significativos. El consumo de alimentos o líquidos ácidos con aluminio mejora la absorción de aluminio, y se ha demostrado que el maltol aumenta la acumulación de aluminio en los tejidos nerviosos y óseos.
Tratamiento
En caso de sospecha de una ingesta repentina de una gran cantidad de aluminio, el único tratamiento es el mesilato de deferoxamina que se puede administrar para ayudar a eliminar el aluminio del cuerpo por quelación. Sin embargo, esto debe aplicarse con precaución, ya que reduce no solo los niveles corporales de aluminio, sino también los de otros metales como el cobre o el hierro. Nutricionalmente, el tratamiento es similar al de otros metales tóxicos e incluye la eliminación de las fuentes de aluminio del medio ambiente, la mejora de la producción de energía celular, la mejora de la actividad de los órganos de eliminación y la quelación del aluminio con nutrientes.
Efectos ambientales
Altos niveles de aluminio ocurren cerca de las ciudades mineras; pequeñas cantidades de aluminio son liberadas al medio ambiente en las plantas de energía o incineradores que funcionan con carbón. El aluminio en el aire es arrastrado por la lluvia o normalmente se asienta, pero pequeñas partículas de aluminio permanecen en el aire durante mucho tiempo.
La precipitación ácida es el principal factor natural para movilizar el aluminio a partir de fuentes naturales y la principal razón de los efectos ambientales del aluminio; sin embargo, el principal factor de presencia de aluminio en la sal y el agua dulce son los procesos industriales que también liberan aluminio en el aire.
En el agua, el aluminio actúa como un agente toxi en los animales que respiran branquias, como los peces, al causar la pérdida de iones plasmáticos y hemolinfáticos que conducen a la falla osmoregulatoria. Los complejos orgánicos de aluminio pueden absorberse fácilmente e interferir con el metabolismo en mamíferos y aves, aunque esto rara vez sucede en la práctica.
El aluminio es uno de los principales factores que reducen el crecimiento de las plantas en suelos ácidos. Aunque generalmente es inofensivo para el crecimiento de la planta en suelos con pH neutro, la concentración en los suelos ácidos de los cationes Al tóxicos aumenta y altera el crecimiento y la función de la raíz. El trigo ha desarrollado una tolerancia al aluminio, liberando compuestos orgánicos que se unen a los dañinos cationes de aluminio. Se cree que el sorgo tiene el mismo mecanismo de tolerancia.
La producción de aluminio posee sus propios desafíos para el medio ambiente en cada paso del proceso de producción. El mayor desafío son las emisiones de gases de efecto invernadero. Estos gases son el resultado del consumo eléctrico de las fundiciones y los subproductos del procesamiento. Los más potentes de estos gases son los perfluorocarbonos del proceso de fundición. El dióxido de azufre liberado es uno de los principales precursores de la lluvia ácida.
Un informe científico español de 2001 afirmó que el hongo Geotrichum candidum consume el aluminio en discos compactos. Otros informes se refieren a ese informe y no hay investigación original de apoyo. Mejor documentada, la bacteria Pseudomonas aeruginosa y el hongo Cladosporium resinae se detectan comúnmente en los tanques de combustible de los aviones que usan combustibles a base de kerosene (no avgas), y los cultivos de laboratorio pueden degradar el aluminio. Sin embargo, estas formas de vida no atacan ni consumen directamente el aluminio; más bien, el metal está corroído por productos de desecho microbianos.