Agua
Definición
El agua es una sustancia química transparente, insípida, inodoro y casi incolora que es el principal constituyente de las corrientes de la Tierra, lagos y océanos, y los fluidos de la mayoría de los organismos vivos. Su fórmula química es H 2 O , lo que significa que cada una de sus moléculas contiene un oxígeno y dos átomos de hidrógeno conectados por enlaces covalentes. Estrictamente hablando, agua se refiere al estado líquido de una sustancia que prevalece a la temperatura y presión ambiental estándar; pero a menudo también se refiere a su estado sólido (hielo) o su estado gaseoso (vapor o vapor de agua). También ocurre en la naturaleza como nieve, glaciares, hielo y icebergs, nubes, niebla, rocío, acuíferos y humedad atmosférica.
El agua cubre el 71% de la superficie de la Tierra. Es vital para todas las formas de vida conocidas. En la Tierra, el 96.5% del agua de la corteza terrestre se encuentra en mares y océanos, 1.7% en aguas subterráneas, 1.7% en glaciares y casquetes de hielo de la Antártida y Groenlandia, una pequeña fracción en otras grandes masas de agua, y 0.001% en el aire como vapor, nubes (formadas por hielo y agua líquida suspendidas en el aire) y precipitación. Solo el 2.5% de esta agua es agua dulce, y el 98.8% de esa agua está en hielo (excepto el hielo en las nubes) y agua subterránea. Menos del 0.3% de toda el agua dulce se encuentra en ríos, lagos y la atmósfera, y una cantidad aún menor del agua dulce de la Tierra (0.003%) está contenida en cuerpos biológicos y productos manufacturados. Una mayor cantidad de agua se encuentra en el interior de la tierra.
El agua en la Tierra se mueve continuamente a través del ciclo del agua de evaporación y transpiración (evapotranspiración), condensación, precipitación y escorrentía, generalmente llegando al mar. La evaporación y la transpiración contribuyen a la precipitación sobre la tierra. Grandes cantidades de agua también se combinan químicamente o se adsorben en minerales hidratados.
El agua potable segura es esencial para los seres humanos y otras formas de vida a pesar de que no proporciona calorías ni nutrientes orgánicos. El acceso al agua potable ha mejorado en las últimas décadas en casi todas partes del mundo, pero aproximadamente mil millones de personas aún carecen de acceso a agua potable y más de 2.500 millones carecen de acceso a servicios de saneamiento adecuados. Sin embargo, algunos observadores estiman que en 2025 más de la mitad de la población mundial enfrentará una vulnerabilidad basada en el agua. Un informe, emitido en noviembre de 2009, sugiere que para 2030, en algunas regiones en desarrollo del mundo, la demanda de agua superará la oferta en un 50%.
El agua juega un papel importante en la economía mundial. Aproximadamente el 70% del agua dulce utilizada por los seres humanos se destina a la agricultura. La pesca en sal y cuerpos de agua dulce es una fuente importante de alimentos para muchas partes del mundo. Gran parte del comercio de productos básicos a larga distancia (como el petróleo y el gas natural) y productos manufacturados se transporta en botes a través de mares, ríos, lagos y canales. Se usan grandes cantidades de agua, hielo y vapor para enfriar y calentar, en la industria y en el hogar. El agua es un excelente solvente para una amplia variedad de sustancias químicas; como tal, es ampliamente utilizado en procesos industriales, y en la cocina y el lavado. El agua también es fundamental para muchos deportes y otras formas de entretenimiento, como la natación, el paseo en bote, las carreras de botes, el surf, la pesca deportiva y el buceo.
Etimología
La palabra "agua" proviene del inglés antiguo "wæter", del proto-germánico "* watar" (fuente también del antiguo sajón "watar", frisón antiguo "wetir", holandés "agua", antiguo alto alemán "wazzar", alemán "Wasser", antiguo nórdico "vatn", gótico "wato"), de proto-indoeuropeo "* wod-or", sufijo de raíz "* wed-" ("agua", "mojado").
Propiedades químicas y físicas
Agua ( H
2 O) es un compuesto inorgánico polar que está a temperatura ambiente, un líquido insípido e inodoro, casi incoloro con un toque de azul. Este calcogenuro de hidrógeno más simple es, con mucho, el compuesto químico más estudiado y se describe como el "disolvente universal" por su capacidad de disolver muchas sustancias. Esto le permite ser el "solvente de la vida". Es la única sustancia común que existe como un sólido, líquido y gas en condiciones terrestres normales.
2 O) es un compuesto inorgánico polar que está a temperatura ambiente, un líquido insípido e inodoro, casi incoloro con un toque de azul. Este calcogenuro de hidrógeno más simple es, con mucho, el compuesto químico más estudiado y se describe como el "disolvente universal" por su capacidad de disolver muchas sustancias. Esto le permite ser el "solvente de la vida". Es la única sustancia común que existe como un sólido, líquido y gas en condiciones terrestres normales.
Estados
El agua es un líquido a las temperaturas y presiones más adecuadas para la vida. Específicamente, a una presión estándar de 1 atm, el agua es un líquido entre 0 y 100 ° C (32 y 212 ° F). El aumento de la presión reduce ligeramente el punto de fusión, que es de aproximadamente -5 ° C (23 ° F) a 600 atm y -22 ° C (-8 ° F) a 2100 atm. Este efecto es relevante, por ejemplo, para el patinaje sobre hielo, para los lagos enterrados de la Antártida y para el movimiento de los glaciares. (A presiones superiores a 2100 atm el punto de fusión aumenta rápidamente de nuevo, y el hielo toma varias formas exóticas que no existen a presiones más bajas).
El aumento de la presión tiene un efecto más dramático en el punto de ebullición, es decir, alrededor de 374 ° C (705 ° F) a 220 atm. Este efecto es importante en, entre otras cosas, los respiraderos hidrotermales de aguas profundas y los géiseres, la cocción a presión y el diseño de los motores de vapor. En la cima del Monte Everest, donde la presión atmosférica es de aproximadamente 0.34 atm, el agua hierve a 68 ° C (154 ° F).
A presiones muy bajas (por debajo de 0,006 atm), el agua no puede existir en estado líquido y pasa directamente de sólido a gas por sublimación, un fenómeno explotado en la liofilización de los alimentos. A presiones muy altas (más de 221 atm), los estados de líquido y gas ya no se distinguen, un estado llamado vapor supercrítico.
El agua también difiere de la mayoría de los líquidos en que se vuelve menos densa a medida que se congela. La densidad máxima de agua en su forma líquida (a 1 atm) es de 1,000 kg / m (62,43 lb / pies cúbicos); eso ocurre a 3.98 ° C (39.16 ° F). La densidad del hielo es de 917 kg / m (57.25 lb / cu ft). Por lo tanto, el agua se expande un 9% en volumen a medida que se congela, lo que explica el hecho de que el hielo flota sobre el agua líquida.
Los detalles de la naturaleza química exacta del agua líquida no se conocen bien; algunas teorías sugieren que el comportamiento inusual del agua es como resultado de tener 2 estados líquidos.
Sabor y olor
El agua pura generalmente se describe como insípida e inodoro, aunque los humanos tienen sensores específicos que pueden sentir la presencia de agua en sus bocas, y se sabe que las ranas lo pueden oler. Sin embargo, el agua de fuentes ordinarias (incluido el agua mineral embotellada) generalmente tiene muchas sustancias disueltas, que pueden darle diferentes sabores y olores. Los seres humanos y otros animales han desarrollado sentidos que les permiten evaluar la potabilidad del agua al evitar agua demasiado salada o pútrida.
Color y apariencia
El color aparente de los cuerpos de agua naturales (y piscinas) a menudo está más determinado por los sólidos disueltos y suspendidos, o por el reflejo del cielo, que por el agua misma.
La luz en el espectro electromagnético visible puede atravesar un par de metros de agua pura (o hielo) sin una absorción significativa, por lo que se ve transparente e incoloro. Por lo tanto, las plantas acuáticas, las algas y otros organismos fotosintéticos pueden vivir en el agua hasta cientos de metros de profundidad, porque la luz solar puede alcanzarlos. El vapor de agua es esencialmente invisible como un gas.
Sin embargo, a través de un espesor de 10 metros (33 pies) o más, el color intrínseco del agua (o hielo) es visiblemente turquesa (azul verdoso), ya que su espectro de absorción tiene un mínimo nítido con el correspondiente color de la luz (1/227 m a 418 nm). El color se vuelve cada vez más fuerte y más oscuro a medida que aumenta el grosor. (Prácticamente no llega la luz del sol a las partes de los océanos por debajo de 1,000 metros (3,300 pies) de profundidad). La luz infrarroja y ultravioleta, por otro lado, es fuertemente absorbida por el agua.
El índice de refracción del agua líquida (1.333 a 20 ° C (68 ° F)) es mucho más alto que el del aire (1.0), similar a los de alcanos y etanol, pero más bajo que los de glicerol (1.473), benceno (1.501 ), disulfuro de carbono (1.627) y tipos comunes de vidrio (1.4 a 1.6). El índice de refracción del hielo (1.31) es menor que el del agua líquida.
Polaridad y enlaces de hidrógeno
Como la molécula de agua no es lineal y el átomo de oxígeno tiene una electronegatividad más alta que los átomos de hidrógeno, es una molécula polar con un momento dipolar eléctrico: el átomo de oxígeno tiene una ligera carga negativa, mientras que los átomos de hidrógeno son ligeramente positivos. El agua es un buen solvente polar, que disuelve muchas sales y moléculas orgánicas hidrofílicas como azúcares y alcoholes simples como el etanol. La mayoría de los ácidos se disuelven en agua para producir los aniones correspondientes. Muchas sustancias en organismos vivos, como proteínas, ADN y polisacáridos, se disuelven en agua. El agua también disuelve muchos gases, como el oxígeno y el dióxido de carbono, y este último produce el chisporroteo de las bebidas carbonatadas, los vinos espumosos y las cervezas.
Por otro lado, muchas sustancias orgánicas (como grasas y aceites y alcanos) son hidrófobas, es decir, insolubles en agua. Muchas sustancias inorgánicas también son insolubles, incluida la mayoría de los óxidos, sulfuros y silicatos metálicos.
Debido a su polaridad, una molécula de agua en estado líquido o sólido puede formar hasta cuatro enlaces de hidrógeno con moléculas vecinas. Estos enlaces son la causa de la alta tensión superficial y las fuerzas capilares del agua. La acción capilar se refiere a la tendencia del agua a subir un tubo estrecho contra la fuerza de la gravedad. Todas las plantas vasculares, como los árboles, confían en esta propiedad.
Los enlaces de hidrógeno también son la razón por la cual los puntos de fusión y ebullición del agua son mucho más altos que los de otros compuestos análogos como el sulfuro de hidrógeno ( H
2 S). También explican su capacidad calorífica excepcionalmente alta (aproximadamente 4.2 J / g / K), el calor de fusión (alrededor de 333 J / g), el calor de vaporización (2257 J / g) y la conductividad térmica (entre 0.561 y 0.679 W / m / K). Estas propiedades hacen que el agua sea más efectiva para moderar el clima de la Tierra al almacenar calor y transportarlo entre los océanos y la atmósfera. Los enlaces de hidrógeno del agua son de intensidad moderada, alrededor de 23 kJ / mol (en comparación con un enlace OH covalente a 492 kJ / mol). De esto, se estima que el 90% del enlace de hidrógeno es atribuible a la electrostática, mientras que el 10% restante refleja un carácter covalente parcial.
2 S). También explican su capacidad calorífica excepcionalmente alta (aproximadamente 4.2 J / g / K), el calor de fusión (alrededor de 333 J / g), el calor de vaporización (2257 J / g) y la conductividad térmica (entre 0.561 y 0.679 W / m / K). Estas propiedades hacen que el agua sea más efectiva para moderar el clima de la Tierra al almacenar calor y transportarlo entre los océanos y la atmósfera. Los enlaces de hidrógeno del agua son de intensidad moderada, alrededor de 23 kJ / mol (en comparación con un enlace OH covalente a 492 kJ / mol). De esto, se estima que el 90% del enlace de hidrógeno es atribuible a la electrostática, mientras que el 10% restante refleja un carácter covalente parcial.
Conductividad eléctrica y electrólisis
El agua pura tiene una baja conductividad eléctrica, que aumenta con la disolución de una pequeña cantidad de material iónico, como la sal común.
El agua líquida se puede dividir en los elementos de hidrógeno y oxígeno al pasar una corriente eléctrica a través de ella, un proceso llamado electrólisis. La descomposición requiere más energía que el calor liberado por el proceso inverso (285.8 kJ / mol o 15.9 MJ / kg).
Propiedades mecánicas
Se puede suponer que el agua líquida es incompresible para la mayoría de los propósitos: su compresibilidad varía de 4.4 a 5.1 × 10 Pa en condiciones normales. Incluso en los océanos a 4 km de profundidad, donde la presión es de 400 atm, el agua sufre solo un descenso del 1.8% en el volumen.
La viscosidad del agua es de aproximadamente 10 Pa • s o 0.01 poise a 20 ° C (68 ° F), y la velocidad del sonido en agua líquida oscila entre 1,400 y 1,540 metros por segundo (4,600 y 5,100 ft / s) dependiendo de la temperatura . El sonido viaja largas distancias en el agua con poca atenuación, especialmente a bajas frecuencias (aproximadamente 0,03 dB / km para 1 kHz), una propiedad que es explotada por cetáceos y humanos para la comunicación y la detección del entorno (sonar).
Reactividad
Los elementos que son más electropositivos que el hidrógeno como el litio, el sodio, el calcio, el potasio y el cesio desplazan el hidrógeno del agua, formando hidróxidos y liberando hidrógeno.
En la tierra
La hidrología es el estudio del movimiento, la distribución y la calidad del agua en toda la Tierra. El estudio de la distribución del agua es hidrografía. El estudio de la distribución y movimiento de aguas subterráneas es hidrogeología, de glaciares es glaciología, de aguas interiores es limnología y la distribución de océanos es oceanografía. Los procesos ecológicos con hidrología están en el foco de la ecohidrología.
La masa colectiva de agua que se encuentra en, debajo y sobre la superficie de un planeta se denomina hidrosfera. El volumen aproximado de agua de la Tierra (el suministro total de agua del mundo) es de 1,38 billones de kilómetros cúbicos (321 × 10 cu mi).
El agua líquida se encuentra en cuerpos de agua, como un océano, mar, lago, río, arroyo, canal, estanque o charco. La mayoría del agua en la Tierra es agua de mar. El agua también está presente en la atmósfera en estados sólidos, líquidos y de vapor. También existe como agua subterránea en los acuíferos.
El agua es importante en muchos procesos geológicos. El agua subterránea está presente en la mayoría de las rocas, y la presión de estas aguas subterráneas afecta los patrones de fallas. El agua en el manto es responsable del derretimiento que produce los volcanes en las zonas de subducción. En la superficie de la Tierra, el agua es importante en los procesos de meteorización física y química. El agua, y en menor medida, pero aún en gran medida, el hielo, también son responsables de una gran cantidad de transporte de sedimentos que se produce en la superficie de la tierra. La deposición del sedimento transportado forma muchos tipos de rocas sedimentarias, que constituyen el registro geológico de la historia de la Tierra.
El ciclo del agua
El ciclo del agua (conocido científicamente como el ciclo hidrológico ) se refiere al intercambio continuo de agua dentro de la hidrósfera, entre la atmósfera, el agua del suelo, las aguas superficiales, las aguas subterráneas y las plantas.
El agua se mueve perpetuamente a través de cada una de estas regiones en el ciclo del agua y consiste en seguir los siguientes procesos de transferencia:
- la evaporación de los océanos y otros cuerpos de agua en el aire y la transpiración de plantas terrestres y animales en el aire.
- precipitación, del vapor de agua que se condensa del aire y cae a la tierra o al océano.
- escorrentía de la tierra generalmente llegando al mar.
La mayoría del vapor de agua sobre los océanos vuelve a los océanos, pero los vientos transportan vapor de agua sobre la tierra a la misma velocidad que la escorrentía hacia el mar, alrededor de 47 Tt por año. Sobre la tierra, la evaporación y la transpiración contribuyen otras 72 Tt por año. La precipitación, a una tasa de 119 Tt por año sobre la tierra, tiene varias formas: generalmente lluvia, nieve y granizo, con alguna contribución de la niebla y el rocío. El rocío es pequeñas gotas de agua que se condensan cuando una alta densidad de vapor de agua se encuentra con una superficie fría. El rocío generalmente se forma en la mañana cuando la temperatura es más baja, justo antes del amanecer y cuando la temperatura de la superficie de la tierra comienza a aumentar. El agua condensada en el aire también puede refractar la luz solar para producir arcoiris.
La escorrentía de agua a menudo se acumula sobre las cuencas hidrográficas que desembocan en los ríos. Un modelo matemático utilizado para simular el flujo de ríos o arroyos y calcular los parámetros de calidad del agua es un modelo de transporte hidrológico. Algo de agua se desvía hacia el riego para la agricultura. Los ríos y los mares ofrecen la oportunidad de viajar y comerciar. A través de la erosión, la escorrentía da forma al medio ambiente creando valles fluviales y deltas que proporcionan un suelo rico y nivelado para el establecimiento de centros de población. Una inundación ocurre cuando un área de tierra, generalmente baja, está cubierta de agua. Es cuando un río se desborda de sus riberas o la inundación proviene del mar. Una sequía es un período prolongado de meses o años cuando una región nota una deficiencia en el suministro de agua. Esto ocurre cuando una región recibe constantemente precipitación por debajo del promedio.
Almacenamiento de agua dulce
Algunas aguas de escorrentía quedan atrapadas durante períodos de tiempo, por ejemplo, en lagos. A gran altitud, durante el invierno y en el extremo norte y sur, la nieve se acumula en capas de hielo, paquetes de nieve y glaciares. El agua también se infiltra en el suelo y penetra en los acuíferos. Estas aguas subterráneas luego vuelven a la superficie en manantiales, o más espectacularmente en aguas termales y géiseres. El agua subterránea también se extrae artificialmente en pozos. Este almacenamiento de agua es importante, ya que el agua limpia y fresca es esencial para la vida humana y otras basadas en la tierra. En muchas partes del mundo, es escaso.
Agua de mar y mareas
El agua de mar contiene aproximadamente 3,5% de cloruro de sodio en promedio, más pequeñas cantidades de otras sustancias. Las propiedades físicas del agua de mar difieren del agua dulce en algunos aspectos importantes. Se congela a una temperatura más baja (aproximadamente -1.9 ° C (28.6 ° F)) y su densidad aumenta con la disminución de la temperatura hasta el punto de congelación, en lugar de alcanzar la densidad máxima a una temperatura superior al punto de congelación. La salinidad del agua en los principales mares varía desde alrededor del 0,7% en el Mar Báltico hasta el 4,0% en el Mar Rojo. (El Mar Muerto, conocido por sus niveles de salinidad ultra alta de entre 30-40%, es realmente un lago salado).
Las mareas son el ascenso y descenso cíclico de los niveles locales del mar causados por las fuerzas de marea de la Luna y el Sol que actúa sobre los océanos. Las mareas causan cambios en la profundidad de las masas de agua marinas y estuarinas y producen corrientes oscilantes conocidas como corrientes de marea. La marea cambiante producida en un lugar determinado es el resultado de las posiciones cambiantes de la Luna y el Sol en relación con la Tierra, junto con los efectos de la rotación de la Tierra y la batimetría local. La franja de orilla del mar que se sumerge con la marea alta y que está expuesta durante la marea baja, la zona intermareal, es un importante producto ecológico de las mareas oceánicas.
Efectos en la vida
Desde un punto de vista biológico, el agua tiene muchas propiedades distintas que son fundamentales para la proliferación de la vida. Lleva a cabo esta función al permitir que los compuestos orgánicos reaccionen de forma que finalmente permitan la replicación. Todas las formas de vida conocidas dependen del agua. El agua es vital como disolvente en el que muchos de los solutos del cuerpo se disuelven y como parte esencial de muchos procesos metabólicos en el cuerpo. El metabolismo es la suma total de anabolismo y catabolismo. En el anabolismo, el agua se elimina de las moléculas (a través de la energía que requiere reacciones químicas enzimáticas) para desarrollar moléculas más grandes (por ejemplo, almidones, triglicéridos y proteínas para el almacenamiento de combustibles e información). En el catabolismo, el agua se usa para romper enlaces con el fin de generar moléculas más pequeñas (por ejemplo, glucosa, ácidos grasos y aminoácidos que se utilizarán para combustibles para uso energético u otros fines). Sin agua, estos procesos metabólicos particulares no podrían existir.
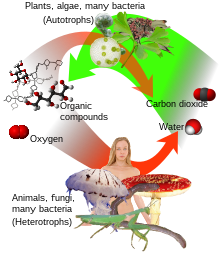
El agua es fundamental para la fotosíntesis y la respiración. Las células fotosintéticas usan la energía del sol para separar el hidrógeno del agua del oxígeno. El hidrógeno se combina con CO 2 (absorbido del aire o del agua) para formar glucosa y liberar oxígeno. Todas las células vivas utilizan tales combustibles y oxidan el hidrógeno y el carbono para capturar la energía del sol y reformar el agua y el CO 2 en el proceso (respiración celular).
El agua también es fundamental para la neutralidad ácido-base y la función enzimática. Un ácido, un donador de iones de hidrógeno (H, es decir, un protón), puede ser neutralizado por una base, un aceptor de protones tal como un ion hidróxido (OH) para formar agua. El agua se considera neutra, con un pH (el logaritmo negativo de la concentración de iones de hidrógeno) de 7. Los ácidos tienen valores de pH menores que 7 mientras que las bases tienen valores mayores a 7.
Formas de vida acuática
Las aguas de la superficie de la Tierra están llenas de vida. Las primeras formas de vida aparecieron en el agua; casi todos los peces viven exclusivamente en el agua, y hay muchos tipos de mamíferos marinos, como delfines y ballenas. Algunos tipos de animales, como los anfibios, pasan porciones de sus vidas en el agua y porciones en la tierra. Las plantas como algas marinas y algas crecen en el agua y son la base de algunos ecosistemas submarinos. El plancton es generalmente la base de la cadena alimentaria oceánica.
Los vertebrados acuáticos deben obtener oxígeno para sobrevivir, y lo hacen de diversas maneras. Los peces tienen branquias en lugar de pulmones, aunque algunas especies de peces, como el pez pulmonado, tienen ambas. Los mamíferos marinos, como los delfines, las ballenas, las nutrias y las focas, necesitan emerger periódicamente para respirar aire. Algunos anfibios pueden absorber oxígeno a través de su piel. Los invertebrados exhiben una amplia gama de modificaciones para sobrevivir en aguas pobremente oxigenadas, incluyendo tubos de respiración (ver sifones de insectos y moluscos) y branquias ( Carcinus ). Sin embargo, como la vida de los invertebrados evolucionó en un hábitat acuático, la mayoría tiene poca o ninguna especialización para la respiración en el agua.
Efectos sobre la civilización humana
La civilización históricamente ha florecido alrededor de los ríos y las principales vías fluviales; Mesopotamia, la llamada cuna de la civilización, estaba situada entre los principales ríos Tigris y Éufrates; la antigua sociedad de los egipcios dependía enteramente del Nilo. Roma también se fundó a orillas del río Tiber italiano. Grandes metrópolis como Rotterdam, Londres, Montreal, París, Nueva York, Buenos Aires, Shanghai, Tokio, Chicago y Hong Kong deben su éxito en parte a su fácil acceso a través del agua y la consiguiente expansión del comercio. Las islas con puertos de agua seguros, como Singapur, han florecido por la misma razón. En lugares como el norte de África y el Medio Oriente, donde el agua es más escasa, el acceso al agua potable fue y es un factor importante en el desarrollo humano.
Salud y contaminación
El agua apta para el consumo humano se llama agua potable o agua potable. El agua que no es potable puede hacerse potable por filtración o destilación, o por una variedad de otros métodos.
El agua que no es apta para beber pero que no es dañina para los humanos cuando se usa para nadar o bañarse se conoce con distintos nombres distintos de agua potable o agua potable, y algunas veces se denomina agua segura o "segura para bañarse". El cloro es un irritante de la piel y las membranas mucosas que se utiliza para hacer que el agua sea segura para bañarse o beber. Su uso es altamente técnico y generalmente es monitoreado por las regulaciones gubernamentales (típicamente 1 parte por millón (ppm) de agua potable, y 1-2 ppm de cloro aún no reaccionado con impurezas para el agua de baño). El agua para el baño se puede mantener en condiciones microbiológicas satisfactorias utilizando desinfectantes químicos como cloro u ozono o mediante el uso de luz ultravioleta.
En los Estados Unidos, las formas no potables de aguas residuales generadas por humanos pueden denominarse aguas grises, que son tratables y, por lo tanto, fácilmente potabilizables nuevamente, y las aguas negras, que generalmente contienen aguas residuales y otras formas de desechos que requieren tratamiento adicional. Para ser reutilizable. Greywater compone 50-80% de las aguas residuales residenciales generadas por los equipos de saneamiento de un hogar (fregaderos, duchas y escurrimientos de cocina, pero no inodoros, que generan aguas negras). Estos términos pueden tener diferentes significados en otros países y culturas.
Este recurso natural es cada vez más escaso en ciertos lugares, y su disponibilidad es una gran preocupación social y económica. En la actualidad, alrededor de mil millones de personas en todo el mundo beben habitualmente agua no saludable. La mayoría de los países aceptaron el objetivo de reducir a la mitad para el año 2015 el número de personas en todo el mundo que no tienen acceso a agua potable y saneamiento durante la cumbre G8 Evian de 2003. Incluso si se cumple este objetivo difícil, todavía dejará a más de medio billón de personas sin acceso a agua potable segura y más de mil millones sin acceso a saneamiento adecuado. La mala calidad del agua y el mal saneamiento son mortales; alrededor de cinco millones de muertes al año son causadas por agua potable contaminada. La Organización Mundial de la Salud estima que el agua potable podría prevenir 1,4 millones de muertes infantiles por diarrea cada año.
El agua, sin embargo, no es un recurso finito (lo que significa que la disponibilidad de agua es limitada), sino que se recircula como agua potable en la precipitación en cantidades de varios órdenes de magnitud superiores al consumo humano. Por lo tanto, es la cantidad relativamente pequeña de agua en reserva en la tierra (aproximadamente el 1% de nuestro suministro de agua potable, que se repone en acuíferos cada 1 a 10 años), que es un recurso no renovable, y es, más bien, la distribución de agua potable y de riego que es escasa, en lugar de la cantidad real que existe en la tierra. Los países pobres en agua usan la importación de bienes como el principal método de importación de agua (para dejar suficiente para el consumo humano local), ya que el proceso de fabricación utiliza entre 10 y 100 veces más masas de productos en agua.
En el mundo en desarrollo, el 90% de todas las aguas residuales aún no se tratan en los ríos y arroyos locales. Unos 50 países, con aproximadamente un tercio de la población mundial, también sufren estrés hídrico medio o alto, y 17 de ellos extraen más agua anualmente de lo que se recarga a través de sus ciclos de agua naturales. La cepa no solo afecta cuerpos superficiales de agua dulce como ríos y lagos, sino que también degrada los recursos de agua subterránea.
Usos humanos
Agricultura
Distribución de agua en riego por goteo subsuperficial
El uso más importante del agua en la agricultura es el riego, que es un componente clave para producir alimentos suficientes. El riego absorbe hasta el 90% del agua extraída en algunos países en desarrollo y proporciones significativas en países más desarrollados económicamente (en los Estados Unidos, el 30% del uso de agua dulce es para irrigación).
Hace cincuenta años, la percepción común era que el agua era un recurso infinito. En ese momento, había menos de la mitad de la cantidad actual de personas en el planeta. Las personas no eran tan ricas como en la actualidad, consumían menos calorías y comían menos carne, por lo que se necesitaba menos agua para producir sus alimentos. Requerían un tercio del volumen de agua que actualmente tomamos de los ríos. Hoy, la competencia por la cantidad fija de recursos hídricos es mucho más intensa, dando lugar al concepto de agua máxima. Esto se debe a que en la actualidad hay casi siete mil millones de personas en el planeta, su consumo de carne y verduras sedientas de agua está aumentando y existe una creciente competencia por el agua de la industria, la urbanización y los cultivos de biocombustibles. En el futuro, se necesitará aún más agua para producir alimentos porque la Tierra '
Una evaluación de la gestión del agua en la agricultura se llevó a cabo en 2007 por el Instituto Internacional de Gestión del Agua en Sri Lanka para ver si el mundo tenía agua suficiente para proporcionar alimentos a su creciente población. Evaluó la disponibilidad actual de agua para la agricultura a escala global y trazó un mapa de las localidades que sufren de escasez de agua. Descubrió que una quinta parte de la población mundial, más de 1.200 millones, vive en áreas de escasez física de agua, donde no hay suficiente agua para satisfacer todas las demandas. Otros 1.600 millones de personas viven en zonas con escasez económica de agua, donde la falta de inversión en agua o la insuficiencia de la capacidad humana hacen que las autoridades no puedan satisfacer la demanda de agua. El informe encontró que sería posible producir los alimentos requeridos en el futuro, pero esa continuación de hoy ' La producción de alimentos y las tendencias ambientales conducirían a crisis en muchas partes del mundo. Para evitar una crisis mundial del agua, los agricultores tendrán que esforzarse por aumentar la productividad para satisfacer la creciente demanda de alimentos, mientras que la industria y las ciudades encuentran formas de utilizar el agua de manera más eficiente.
La escasez de agua también es causada por la producción de algodón: 1 kg de algodón equivalente a un par de jeans: requiere 10,9 metros cúbicos (380 pies cúbicos) de agua para producir. Mientras que el algodón representa el 2.4% del uso mundial de agua, el agua se consume en regiones que ya están en riesgo de escasez de agua. Se ha causado un daño ambiental importante, como la desaparición del Mar de Aral.
Como un estándar científico
El 7 de abril de 1795, el gramo fue definido en Francia para ser igual al "peso absoluto de un volumen de agua pura igual a un cubo de una centésima de metro, y a la temperatura del hielo que se derrite". Sin embargo, para fines prácticos, se requería un patrón de referencia metálico, mil veces más masivo, el kilogramo. Por lo tanto, se encargó el trabajo para determinar con precisión la masa de un litro de agua. A pesar del hecho de que la definición decretada del gramo especificaba agua a 0 ° C (32 ° F) -una temperatura altamente reproducible- los científicos optaron por redefinir el estándar y realizar sus mediciones a la temperatura de mayor densidad de agua , que se midió en ese momento como 4 ° C (39 ° F).
La escala de temperatura Kelvin del sistema SI se basa en el punto triple del agua, que se define exactamente como 273.16 K (0.01 ° C; 32.02 ° F). La escala es una escala de temperatura absoluta con el mismo incremento que la escala de temperatura Celsius, que originalmente se definió de acuerdo con el punto de ebullición (ajustado a 100 ° C (212 ° F)) y el punto de fusión (ajustado a 0 ° C (32 ° F)) de agua.
El agua natural consiste principalmente en los isótopos hidrógeno-1 y oxígeno-16, pero también hay una pequeña cantidad de isótopos más pesados como el hidrógeno-2 (deuterio). La cantidad de óxidos de deuterio o agua pesada es muy pequeña, pero aún afecta las propiedades del agua. El agua de los ríos y lagos tiende a contener menos deuterio que el agua de mar. Por lo tanto, el agua estándar se define en la especificación del agua del océano medio estándar de Viena.
Para beber
El cuerpo humano contiene de 55% a 78% de agua, dependiendo del tamaño del cuerpo. Para funcionar correctamente, el cuerpo necesita entre uno y siete litros (0.22 y 1.54 galón; 0.26 y 1.85 galones de galón estadounidense) de agua por día para evitar la deshidratación; la cantidad precisa depende del nivel de actividad, temperatura, humedad y otros factores. La mayor parte de esto se ingiere a través de alimentos o bebidas que no sean beber agua pura. No está claro cuánta ingesta de agua necesitan las personas sanas, aunque la mayoría de los especialistas coinciden en que aproximadamente 2 litros (6 a 7 vasos) de agua al día son los mínimos para mantener una hidratación adecuada. La literatura médica favorece un consumo menor, típicamente 1 litro de agua para un hombre promedio, sin incluir los requisitos adicionales debido a la pérdida de líquidos por el ejercicio o el clima cálido.
Para aquellos que tienen riñones saludables, es bastante difícil beber mucha agua, pero (especialmente en climas cálidos y húmedos y durante el ejercicio) es peligroso beber muy poco. Sin embargo, las personas pueden beber mucha más agua de la necesaria mientras se ejercitan, lo que las pone en riesgo de intoxicación con agua (hiperhidratación), que puede ser fatal. La afirmación popular de que "una persona debería consumir ocho vasos de agua por día" parece no tener ninguna base real en la ciencia. Los estudios han demostrado que la ingesta extra de agua, especialmente hasta 500 mililitros (18 imp fl oz; 17 onzas fl oz) a la hora de la comida condujo a la pérdida de peso. La ingesta adecuada de líquidos es útil para prevenir el estreñimiento.
Una recomendación original para la ingesta de agua en 1945 por la Junta de Alimentos y Nutrición del Consejo Nacional de Investigación de Estados Unidos decía: "Un estándar común para personas diversas es de 1 mililitro por cada caloría de alimentos. La mayoría de esta cantidad está contenida en alimentos preparados". El último informe de ingesta de referencia dietética recomendado por el Consejo de Investigación Nacional de los Estados Unidos, en general, se basa en la mediana de la ingesta total de agua de datos de encuestas estadounidenses (incluidas fuentes de alimentos): 3.7 litros (0.81 imp gal; 0.98 US gal) para hombres y 2.7 litros (0.59 imp gal, 0.71 US gal) de agua total para las mujeres, señalando que el agua contenida en los alimentos proporcionó aproximadamente el 19% de la ingestión total de agua en la encuesta.
Específicamente, las mujeres embarazadas y en período de lactancia necesitan líquidos adicionales para mantenerse hidratadas. El Instituto de Medicina (EE. UU.) Recomienda que, en promedio, los hombres consuman 3 litros (0.66 imp gal, 0.79 US gal) y las mujeres 2.2 litros (0.48 imp gal, 0.58 US gal); las mujeres embarazadas deben aumentar el consumo a 2.4 litros (0.53 imp gal, 0.63 US gal) y las mujeres que amamantan deben recibir 3 litros (12 tazas), ya que una cantidad especialmente grande de líquido se pierde durante la lactancia. También se observa que, normalmente, alrededor del 20% de la ingesta de agua proviene de los alimentos, mientras que el resto proviene del agua potable y las bebidas (incluida la cafeína). El agua se excreta del cuerpo en formas múltiples; a través de la orina y las heces, a través de la sudoración y mediante la exhalación de vapor de agua en la respiración. Con esfuerzo físico y exposición al calor, la pérdida de agua aumentará y las necesidades diarias de fluidos también pueden aumentar.
Los humanos requieren agua con pocas impurezas. Las impurezas comunes incluyen sales y óxidos de metales, como cobre, hierro, calcio y plomo, y / o bacterias dañinas, como Vibrio . Algunos solutos son aceptables e incluso deseables para la mejora del sabor y para proporcionar electrolitos necesarios.
El único recurso de agua dulce más grande (por volumen) adecuado para beber es el lago Baikal en Siberia.
Lavado
La propensión del agua a formar soluciones y emulsiones es útil en varios procesos de lavado. El lavado también es un componente importante de varios aspectos de la higiene personal del cuerpo. La mayor parte del uso personal del agua se debe a la ducha, lavar la ropa y lavar los platos, llegando a cientos de litros por día en los países desarrollados.
Transporte
El uso de agua para el transporte de materiales a través de ríos y canales, así como las rutas marítimas internacionales es una parte importante de la economía mundial.
Usos químicos
El agua se usa ampliamente en reacciones químicas como solvente o reactante y menos comúnmente como soluto o catalizador. En las reacciones inorgánicas, el agua es un disolvente común que disuelve muchos compuestos iónicos, así como otros compuestos polares como el amoníaco y compuestos estrechamente relacionados con el agua. En reacciones orgánicas, generalmente no se usa como solvente de reacción, porque no disuelve bien los reactivos y es anfótero (ácido y básico) y nucleofílico. Sin embargo, estas propiedades son a veces deseables. Además, se ha observado la aceleración de las reacciones de Diels-Alder por el agua. El agua supercrítica ha sido recientemente un tema de investigación. El agua supercrítica saturada de oxígeno quema los contaminantes orgánicos de manera eficiente. El vapor de agua se usa para algunos procesos en la industria química. Un ejemplo es la producción de ácido acrílico a partir de acroleína, propileno y propano. El posible efecto del agua en estas reacciones incluye la interacción física y química del agua con el catalizador y la reacción química del agua con los intermedios de la reacción.
De intercambio de calor
El agua y el vapor son un fluido común utilizado para el intercambio de calor, debido a su disponibilidad y alta capacidad de calor, tanto para refrigeración como para calefacción. El agua fría puede estar naturalmente disponible en un lago o en el mar. Es especialmente efectivo para transportar calor por vaporización y condensación de agua debido a su gran calor latente de vaporización. Una desventaja es que los metales que se encuentran comúnmente en industrias como el acero y el cobre se oxidan más rápidamente con agua y vapor no tratados. En casi todas las centrales térmicas, se utiliza agua como fluido de trabajo (utilizado en un circuito cerrado entre la caldera, la turbina de vapor y el condensador) y el refrigerante (utilizado para intercambiar el calor residual por un cuerpo de agua o llevarlo por evaporación en una torre de enfriamiento). En los Estados Unidos, las plantas de energía de enfriamiento es el mayor uso de agua.
En la industria de la energía nuclear, el agua también se puede usar como un moderador de neutrones. En la mayoría de los reactores nucleares, el agua es tanto un refrigerante como un moderador. Esto proporciona una medida de seguridad pasiva, ya que la eliminación del agua del reactor también ralentiza la reacción nuclear. Sin embargo, se prefieren otros métodos para detener una reacción y se prefiere mantener el núcleo nuclear cubierto de agua para asegurar una refrigeración adecuada.
Extinción de fuego
El agua tiene un alto calor de vaporización y es relativamente inerte, lo que lo convierte en un buen fluido extintor de incendios. La evaporación del agua aleja el calor del fuego. Es peligroso usar agua en incendios que involucran aceites y solventes orgánicos, porque muchos materiales orgánicos flotan en el agua y el agua tiende a extender el líquido ardiente.
El uso de agua en la lucha contra incendios también debe tener en cuenta los peligros de una explosión de vapor, que puede ocurrir cuando se usa agua en incendios muy calientes en espacios confinados, y de una explosión de hidrógeno, cuando las sustancias reaccionan con el agua, como ciertos metales o carbón caliente como carbón, carbón o grafito de coque, descomponen el agua y producen gas de agua.
El poder de tales explosiones se vio en el desastre de Chernobyl, aunque el agua involucrada no provenía de la lucha contra incendios en ese momento, sino del propio sistema de refrigeración por agua del reactor. Se produjo una explosión de vapor cuando el sobrecalentamiento extremo del núcleo hizo que el agua se convirtiera en vapor. Una explosión de hidrógeno puede haber ocurrido como resultado de la reacción entre el vapor y el zirconio caliente.
Recreación
Los seres humanos usan el agua para muchos fines recreativos, así como para hacer ejercicio y para practicar deportes. Algunos de estos incluyen natación, esquí acuático, paseos en bote, surf y buceo. Además, algunos deportes, como el hockey sobre hielo y el patinaje sobre hielo, se juegan sobre hielo. Orillas del lago, playas y parques acuáticos son lugares populares para que la gente vaya a relajarse y disfrutar de la recreación. Muchos encuentran que el sonido y la apariencia del agua que fluye son calmantes, y las fuentes y otras características del agua son decoraciones populares. Algunos mantienen los peces y otras formas de vida en acuarios o estanques para mostrar, divertirse y acompañar. Los seres humanos también usan agua para deportes de nieve, como esquí, trineo, motos de nieve o snowboard, que requieren que se congele el agua.
Industria del agua
La industria del agua proporciona servicios de agua potable y aguas residuales (incluido el tratamiento de aguas residuales) a los hogares y la industria. Las instalaciones de suministro de agua incluyen pozos de agua, cisternas para la recolección de agua de lluvia, redes de suministro de agua y plantas de purificación de agua, tanques de agua, torres de agua y tuberías de agua, incluyendo antiguos acueductos. Los generadores atmosféricos de agua están en desarrollo.
El agua potable a menudo se recolecta en manantiales, se extrae de perforaciones artificiales (pozos) en el suelo o se bombea desde lagos y ríos. Construir más pozos en lugares adecuados es, por lo tanto, una posible forma de producir más agua, suponiendo que los acuíferos puedan suministrar un flujo adecuado. Otras fuentes de agua incluyen la recolección de agua de lluvia. El agua puede requerir purificación para consumo humano. Esto puede implicar la eliminación de sustancias no disueltas, sustancias disueltas y microbios dañinos. Los métodos populares se filtran con arena, que solo elimina el material no disuelto, mientras que la cloración y la ebullición matan microbios dañinos. La destilación tiene las tres funciones. Existen técnicas más avanzadas, como la ósmosis inversa. La desalinización de abundante agua de mar es una solución más costosa utilizada en climas áridos costeros.
La distribución de agua potable se realiza a través de sistemas de agua municipales, entrega de buques cisterna o como agua embotellada. Los gobiernos en muchos países tienen programas para distribuir agua a los necesitados sin cargo.
La reducción del uso mediante el consumo de agua potable (potable) solo para el consumo humano es otra opción. En algunas ciudades como Hong Kong, el agua de mar se usa ampliamente para descargar inodoros en toda la ciudad con el fin de conservar los recursos de agua dulce.
La contaminación del agua puede ser el mayor mal uso del agua; en la medida en que un contaminante limita otros usos del agua, se convierte en un desperdicio del recurso, independientemente de los beneficios para el que contamina. Al igual que otros tipos de contaminación, esto no entra en la contabilidad estándar de los costos de mercado, ya que se concibe como externalidades que el mercado no puede contabilizar. Por lo tanto, otras personas pagan el precio de la contaminación del agua, mientras que las ganancias de las empresas privadas no se redistribuyen a la población local, víctimas de esta contaminación. Los productos farmacéuticos que consumen los humanos a menudo terminan en las vías fluviales y pueden tener efectos perjudiciales en la vida acuática si se bioacumulan y si no son biodegradables.
Las aguas residuales municipales e industriales generalmente se tratan en plantas de tratamiento de aguas residuales. La mitigación de la escorrentía superficial contaminada se aborda a través de una variedad de técnicas de prevención y tratamiento. ( Ver Escorrentía superficial # Mitigación y tratamiento).
Aplicaciones industriales
Muchos procesos industriales dependen de reacciones que utilizan productos químicos disueltos en agua, suspensión de sólidos en lodos de agua o el uso de agua para disolver y extraer sustancias, o para lavar productos o procesar equipos. Procesos como la minería, la fabricación de pasta química, el blanqueo de pulpa, la fabricación de papel, la producción textil, el teñido, la impresión y el enfriamiento de plantas de energía utilizan grandes cantidades de agua, requieren una fuente de agua especializada y a menudo causan una importante contaminación del agua.
El agua se usa en la generación de energía. La hidroelectricidad es la electricidad que se obtiene de la energía hidroeléctrica. La energía hidroeléctrica proviene del agua que impulsa una turbina de agua conectada a un generador. La hidroelectricidad es una fuente de energía renovable de bajo costo y no contaminante. La energía es suministrada por el movimiento del agua. Normalmente, una presa se construye en un río, creando un lago artificial detrás de ella. El agua que sale del lago se ve forzada a través de turbinas que giran generadores.
El agua a presión se usa en chorros de agua y chorros de agua. Además, las pistolas de agua a muy alta presión se utilizan para cortes precisos. Funciona muy bien, es relativamente seguro y no es dañino para el medio ambiente. También se usa para enfriar la maquinaria para evitar el sobrecalentamiento o para evitar el sobrecalentamiento de las hojas de la sierra.
El agua también se usa en muchos procesos y máquinas industriales, como la turbina de vapor y el intercambiador de calor, además de su uso como solvente químico. La descarga de agua no tratada de usos industriales es contaminación. La contaminación incluye solutos descargados (contaminación química) y agua refrigerante descargada (contaminación térmica). La industria requiere agua pura para muchas aplicaciones y utiliza una variedad de técnicas de purificación tanto en el suministro de agua como en la descarga.
Procesamiento de alimentos
Hervir, hervir y hervir a fuego lento son métodos populares de cocción que a menudo requieren la inmersión de alimentos en agua o en su estado gaseoso, vapor. El agua también se usa para lavar los platos. El agua también juega muchos papeles críticos en el campo de la ciencia de los alimentos. Es importante que un científico alimentario comprenda las funciones que desempeña el agua en el procesamiento de alimentos para garantizar el éxito de sus productos.
Los solutos como las sales y azúcares que se encuentran en el agua afectan las propiedades físicas del agua. Los puntos de ebullición y congelación del agua se ven afectados por los solutos, así como la presión del aire, que a su vez se ve afectada por la altitud. El agua hierve a temperaturas más bajas con la presión de aire más baja que ocurre en las elevaciones más altas. Un mol de sacarosa (azúcar) por kilogramo de agua aumenta el punto de ebullición del agua en 0.51 ° C (0.918 ° F), y un mol de sal por kg aumenta el punto de ebullición en 1.02 ° C (1.836 ° F); de manera similar, aumentar el número de partículas disueltas reduce el punto de congelación del agua.
Los solutos en el agua también afectan la actividad del agua que afecta muchas reacciones químicas y el crecimiento de microbios en los alimentos. La actividad del agua puede describirse como una relación entre la presión de vapor del agua en una solución y la presión de vapor del agua pura. Los solutos en el agua reducen la actividad del agua; esto es importante saberlo porque la mayor parte del crecimiento bacteriano cesa en niveles bajos de actividad acuática. El crecimiento microbiano no solo afecta la seguridad de los alimentos, sino también la preservación y la vida útil de los mismos.
La dureza del agua también es un factor crítico en el procesamiento de alimentos y puede alterarse o tratarse mediante el uso de un sistema químico de intercambio iónico. Puede afectar drásticamente la calidad de un producto, así como desempeñar un papel en el saneamiento. La dureza del agua se clasifica en función de la concentración de carbonato de calcio que contiene el agua. El agua se clasifica como blanda si contiene menos de 100 mg / l (RU) o menos de 60 mg / l (EE. UU.).
Según un informe publicado por la organización Water Footprint en 2010, un solo kilogramo de carne de vacuno requiere 15 mil litros (3,3 × 10 imp gal, 4,0 × 10 US gal) de agua; sin embargo, los autores también aclaran que este es un promedio global y los factores circunstanciales determinan la cantidad de agua utilizada en la producción de carne.
Uso médico
El agua para inyección está en la lista de medicamentos esenciales de la Organización Mundial de la Salud.
Distribución en la naturaleza
En el universo
Gran parte del agua del universo se produce como un subproducto de la formación de estrellas. La formación de estrellas va acompañada de un fuerte viento exterior de gas y polvo. Cuando este flujo de material eventualmente impacta en el gas circundante, las ondas de choque que se crean comprimen y calientan el gas. El agua observada se produce rápidamente en este gas denso y cálido.
El 22 de julio de 2011, un informe describió el descubrimiento de una gigantesca nube de vapor de agua que contiene "140 billones de veces más agua que todos los océanos de la Tierra combinados" alrededor de un cuásar ubicado a 12 mil millones de años luz de la Tierra. Según los investigadores, el "descubrimiento muestra que el agua ha prevalecido en el universo durante casi toda su existencia".
Se ha detectado agua en nubes interestelares dentro de nuestra galaxia, la Vía Láctea. El agua probablemente también existe en abundancia en otras galaxias, porque sus componentes, hidrógeno y oxígeno, se encuentran entre los elementos más abundantes del universo. Con base en los modelos de la formación y evolución del Sistema Solar y de otros sistemas estelares, es probable que la mayoría de los otros sistemas planetarios tengan ingredientes similares.
Vapor de agua
El agua está presente como vapor en:
- Atmósfera del Sol: en cantidades detectables
- Atmósfera de Mercurio: 3.4% y grandes cantidades de agua en la exosfera de Mercurio
- Ambiente de Venus: 0.002%
- La atmósfera de la Tierra: ≈0.40% sobre la atmósfera completa, típicamente 1-4% en la superficie; así como el de la Luna en cantidades traza
- Atmósfera de Marte: 0.03%
- Ambiente de Ceres
- Atmósfera de Júpiter: 0.0004% - solo en hielos; y el de su luna Europa
- Atmósfera de Saturno: solo en hielos; y el de sus lunas Titán (estratosférico), Encelado: 91% y Dione (exosfera)
- Atmósfera de Urano: en pequeñas cantidades por debajo de 50 bar
- Atmósfera de Neptuno: se encuentra en las capas más profundas
- Ambientes de planetas extrasolares: incluidos los de HD 189733 by HD 209458 b, Tau Boostis b, HAT-P-11b, XO-1b, WASP-12b, WASP-17b y WASP-19b.
- Ambientes estelares: no se limita a estrellas más frías e incluso se detecta en estrellas calientes gigantes como Betelgeuse, Mu Cephei, Antares y Arcturus.
- Discos circunestelares: incluidos los de más de la mitad de estrellas T Tauri como AA Tauri y TW Hydrae, IRC +10216 y APM 08279 + 5255, VY Canis Majoris y S Persei.
Agua líquida
El agua líquida está presente en la Tierra y cubre el 71% de su superficie. El agua líquida también está ocasionalmente presente en pequeñas cantidades en Marte. Los científicos creen que el agua líquida está presente en las lunas de Saturno de Encelado, como un océano de 10 kilómetros de espesor aproximadamente 30-40 kilómetros debajo de la superficie polar sur de Encelado, y Titán, como una capa subsuperficial, posiblemente mezclada con amoníaco. La luna de Júpiter, Europa, tiene características superficiales que sugieren un océano de agua líquida subsuperficial. El agua líquida también puede existir en la luna Ganímedes de Júpiter como una capa intercalada entre el hielo de alta presión y la roca.
Agua helada
El agua está presente como hielo en:
- Marte: bajo el regolito y en los polos.
- Sistema de Tierra-Luna: principalmente como capas de hielo en la Tierra y en cráteres lunares y rocas volcánicas La NASA informó la detección de moléculas de agua por Moon Mineralogy Mapper de la NASA a bordo de la nave Chandrayaan-1 de la Organización de Investigación Espacial de la India en septiembre de 2009.
- Las lunas de Júpiter: la superficie de Europa y también la de Ganímedes
- Saturno: en el sistema de anillos del planeta y en la superficie y el manto de Titán y Encelado
- Sistema de Plutón-Charon
- Cometas y objetos relacionados (cinturón de Kuiper y objetos en la nube de Oort).
Y también puede estar presente en:
- Polos de mercurio
- Ceres
- Tethys
Formas exóticas
El agua y otros volátiles probablemente comprenden gran parte de las estructuras internas de Urano y Neptuno y el agua en las capas más profundas puede estar en forma de agua iónica en la que las moléculas se descomponen en una sopa de iones de hidrógeno y oxígeno, y más profunda aún como superiónica agua en la que el oxígeno cristaliza pero los iones de hidrógeno flotan libremente dentro de la red de oxígeno.
Agua y zona habitable
La existencia de agua líquida, y en menor medida sus formas gaseosa y sólida, en la Tierra son vitales para la existencia de la vida en la Tierra tal como la conocemos. La Tierra está ubicada en la zona habitable del sistema solar; si estuviera un poco más cerca o más lejos del Sol (aproximadamente 5%, o cerca de 8 millones de kilómetros), las condiciones que permiten que las tres formas estén presentes simultáneamente serían mucho menos probables de existir.
La gravedad de la Tierra le permite mantener una atmósfera. El vapor de agua y el dióxido de carbono en la atmósfera proporcionan un amortiguador de temperatura (efecto invernadero) que ayuda a mantener una temperatura superficial relativamente estable. Si la Tierra fuera más pequeña, una atmósfera más delgada permitiría temperaturas extremas, evitando así la acumulación de agua, excepto en los casquetes polares (como en Marte).
La temperatura superficial de la Tierra ha sido relativamente constante durante el tiempo geológico a pesar de los niveles variables de radiación solar entrante (insolación), lo que indica que un proceso dinámico rige la temperatura de la Tierra mediante una combinación de gases de efecto invernadero y albedo atmosférico o de superficie. Esta propuesta se conoce como la hipótesis de Gaia .
El estado del agua en un planeta depende de la presión ambiental, que está determinada por la gravedad del planeta. Si un planeta es suficientemente masivo, el agua sobre él puede ser sólido incluso a altas temperaturas, debido a la alta presión causada por la gravedad, como se observó en los exoplanetas Gliese 436 by GJ 1214 b.
Ley, política y crisis
La política del agua es la política afectada por los recursos hídricos y el agua. Por esta razón, el agua es un recurso estratégico en el mundo y un elemento importante en muchos conflictos políticos. Causa impactos de salud y daño a la biodiversidad.
1.600 millones de personas han accedido a una fuente de agua potable desde 1990. Se calcula que la proporción de personas en los países en desarrollo con acceso a agua potable mejoró del 30% en 1970 al 71% en 1990, 79% en 2000 y 84% en 1990. 2004. Se prevé que esta tendencia continúe. Para reducir a la mitad, para 2015, la proporción de personas sin acceso sostenible al agua potable es uno de los Objetivos de Desarrollo del Milenio. Se proyecta alcanzar este objetivo.
Un informe de 2006 de las Naciones Unidas declaró que "hay suficiente agua para todos", pero que el acceso a él se ve obstaculizado por la mala gestión y la corrupción. Además, las iniciativas mundiales para mejorar la eficacia de la prestación de ayuda, como la Declaración de París sobre la Eficacia de la Ayuda, no han sido asumidas por los donantes del sector del agua tan eficazmente como en educación y salud, lo que podría dejar a múltiples donantes trabajando en proyectos superpuestos y gobiernos receptores sin empoderamiento para actuar.
Los autores de la Evaluación exhaustiva de la gestión del agua en la agricultura de 2007 citaron la mala gobernanza como una razón para algunas formas de escasez de agua. La gobernanza del agua es el conjunto de procesos formales e informales a través de los cuales se toman decisiones relacionadas con la gestión del agua. La buena gobernanza del agua se trata principalmente de saber qué procesos funcionan mejor en un contexto físico y socioeconómico particular. A veces se han cometido errores al tratar de aplicar "planos" que funcionan en el mundo desarrollado a lugares y contextos del mundo en desarrollo. El río Mekong es un ejemplo; una revisión por parte del Instituto Internacional de Gestión del Agua de las políticas en seis países que dependen del río Mekong para el agua descubrió que rara vez se llevaron a cabo análisis exhaustivos y transparentes de costo-beneficio y evaluaciones del impacto ambiental.
El Informe Mundial sobre el Desarrollo del Agua de la ONU (WWDR, 2003) del Programa Mundial de Evaluación del Agua indica que, en los próximos 20 años, se prevé que la cantidad de agua disponible para todos disminuirá en un 30%. Actualmente, el 40% de los habitantes del mundo tiene agua dulce insuficiente para una higiene mínima. Más de 2.2 millones de personas murieron en 2000 por enfermedades transmitidas por el agua (relacionadas con el consumo de agua contaminada) o por la sequía. En 2004, la organización benéfica británica WaterAid informó que un niño muere cada 15 segundos por enfermedades relacionadas con el agua fácilmente prevenibles; a menudo esto significa falta de eliminación de aguas residuales; ver baño.
Las organizaciones que se preocupan por la protección del agua incluyen International Water Association (IWA), WaterAid, Water 1st y American Water Resources Association. El Instituto Internacional de Gestión del Agua emprende proyectos con el objetivo de utilizar una gestión eficaz del agua para reducir la pobreza. Los convenios relacionados con el agua son la Convención de las Naciones Unidas de Lucha contra la Desertificación (CNULD), la Convención Internacional para Prevenir la Contaminación por los Buques, la Convención de las Naciones Unidas sobre el Derecho del Mar y la Convención de Ramsar. El Día Mundial del Agua se celebra el 22 de marzo y el Día Mundial del Océano el 8 de junio.
En cultura
Religión
El agua se considera un purificador en la mayoría de las religiones. Las religiones que incorporan el lavado ritual (ablución) incluyen el cristianismo, el hinduismo, el islam, el judaísmo, el movimiento rastafari, el sintoísmo, el taoísmo y la wicca. La inmersión (o aspersión o affusión) de una persona en el agua es un sacramento central del cristianismo (donde se llama bautismo); también es parte de la práctica de otras religiones, incluido el Islam ( Ghusl ), el judaísmo ( mikvah ) y el sijismo ( Amrit Sanskar ). Además, se realiza un baño ritual en agua pura para los muertos en muchas religiones, incluyendo el Islam y el judaísmo. En el Islam, las cinco oraciones diarias se pueden hacer en la mayoría de los casos después de completar el lavado de ciertas partes del cuerpo usando agua limpia ( wudu ), a menos que no haya agua disponible (ver Tayammum ). En sintoísmo, el agua se utiliza en casi todos los rituales para limpiar a una persona o un área (por ejemplo, en el ritual de misogi ).
En el cristianismo, el agua bendita es agua que ha sido santificada por un sacerdote para el bautismo, la bendición de personas, lugares y objetos, o como un medio para repeler el mal.
Filosofía
El filósofo griego Empédocles sostenía que el agua es uno de los cuatro elementos clásicos junto con el fuego, la tierra y el aire, y se consideraba como el ylem, o sustancia básica del universo. Thales, quien fue retratado por Aristóteles como un astrónomo y un ingeniero, teorizó que la tierra, que es más densa que el agua, emergió del agua. Thales, un monista, creía además que todas las cosas están hechas de agua. Platón cree que la forma del agua es un icosaedro, lo que explica por qué es capaz de fluir fácilmente en comparación con la tierra en forma de cubo.
En la teoría de los cuatro humores corporales, el agua se asocia con la flema, por ser fría y húmeda. El elemento clásico del agua también fue uno de los cinco elementos de la filosofía tradicional china, junto con la tierra, el fuego, la madera y el metal.
El agua también se toma como un modelo a imitar en algunas partes de la filosofía asiática tradicional y popular. La traducción de James Legge en 1891 del Dao De Jing dice: "La excelencia más alta es como la del agua. La excelencia del agua aparece en su beneficio para todas las cosas, y en su ocupación, sin esfuerzo (por el contrario), el lugar bajo que a todos los hombres les desagrada. Por lo tanto (su camino) está cerca del (del) Tao "y" No hay nada en el mundo más suave y débil que el agua, y sin embargo, para atacar cosas que son firmes y fuertes no hay nada que pueda tome precedencia de eso, ya que no hay nada (tan efectivo) para el cual pueda cambiarse ". Guanzi en el capítulo "Shui di" 水 further el capítulo profundiza sobre el simbolismo del agua, proclamando que "el hombre es agua" y atribuyendo cualidades naturales de las personas de diferentes regiones chinas al carácter de los recursos hídricos locales.
Engaño de monóxido de dihidrógeno
El nombre químico del agua, técnicamente correcto pero raramente usado, "monóxido de dihidrógeno", ha sido utilizado en una serie de fraudes y bromas que se burlan del analfabetismo científico. Esto comenzó en 1983, cuando un artículo del Día de los Inocentes apareció en un periódico en Durand, Michigan. La historia falsa consistió en preocupaciones de seguridad sobre la sustancia.
Obtenido de: https://en.wikipedia.org/wiki/Water