Enlace químico
Definición
Un enlace químico es una atracción duradera entre átomos, iones o moléculas que permite la formación de compuestos químicos. El enlace puede ser el resultado de la fuerza de atracción electrostática entre iones con carga opuesta como en enlaces iónicos o mediante el intercambio de electrones como en enlaces covalentes. La fuerza de los enlaces químicos varía considerablemente; existen "enlaces fuertes" o "enlaces primarios", como enlaces covalentes, iónicos y metálicos, y "enlaces débiles" o "enlaces secundarios", como las interacciones dipolo-dipolo, la fuerza de dispersión de Londres y el enlace de hidrógeno.Como las cargas opuestas se atraen a través de una fuerza electromagnética simple, los electrones cargados negativamente que están en órbita alrededor del núcleo y los protones cargados positivamente en el núcleo se atraen entre sí. Un electrón posicionado entre dos núcleos será atraído por ambos, y los núcleos serán atraídos hacia los electrones en esta posición. Esta atracción constituye el vínculo químico. Debido a la naturaleza de onda de materia de los electrones y su masa más pequeña, deben ocupar una cantidad mucho mayor de volumen en comparación con los núcleos, y este volumen ocupado por los electrones mantiene los núcleos atómicos en un enlace relativamente separado, en comparación con el tamaño de los núcleos mismos.
En general, una fuerte unión química está asociada con la compartición o transferencia de electrones entre los átomos participantes. Los átomos en las moléculas, cristales, metales y gases diatómicos -de hecho, la mayor parte del entorno físico que nos rodea- se mantienen unidos por enlaces químicos, que dictan la estructura y las propiedades globales de la materia.
Todos los enlaces se pueden explicar mediante la teoría cuántica, pero, en la práctica, las reglas de simplificación permiten a los químicos predecir la fuerza, la direccionalidad y la polaridad de los enlaces. La regla del octeto y la teoría VSEPR son dos ejemplos. Las teorías más sofisticadas son la teoría del enlace de valencia que incluye la hibridación orbital y la resonancia, y la teoría de la órbita molecular que incluye la combinación lineal de orbitales atómicos y la teoría del campo del ligando. La electrostática se usa para describir las polaridades de los enlaces y los efectos que tienen en las sustancias químicas.
Descripción de los principales tipos de enlaces químicos
Un enlace químico es una atracción entre átomos. Esta atracción puede verse como el resultado de diferentes comportamientos de los electrones más externos o de valencia de los átomos. Estos comportamientos se combinan sin problemas en diversas circunstancias, de modo que no hay una línea clara que se dibuje entre ellos. Sin embargo, sigue siendo útil y habitual diferenciar entre los diferentes tipos de enlace, que dan lugar a diferentes propiedades de la materia condensada.
En la vista más simple de un enlace covalente, uno o más electrones (a menudo un par de electrones) se dibujan en el espacio entre los dos núcleos atómicos. La energía se libera mediante la formación de enlaces. Esto no es una reducción de la energía potencial, ya que la atracción de los dos electrones hacia los dos protones se compensa con las repulsiones electrón-electrón y protón-protón. En cambio, la liberación de energía (y por lo tanto estabilidad del enlace) surge de la reducción en energía cinética debido a que los electrones están en un orbital más espacialmente distribuido (es decir, más largo de longitud de Broglie) en comparación con cada electrón confinado más cerca de su núcleo respectivo . Estos enlaces existen entre dos átomos identificables particulares y tienen una dirección en el espacio, lo que les permite mostrarse como líneas de conexión individuales entre los átomos en los dibujos,
En un enlace covalente polar, uno o más electrones se comparten de forma desigual entre dos núcleos. Los enlaces covalentes a menudo resultan en la formación de pequeñas colecciones de átomos mejor conectados llamados moléculas, que en sólidos y líquidos están unidos a otras moléculas por fuerzas que a menudo son mucho más débiles que los enlaces covalentes que mantienen unidas internamente a las moléculas. Dichos enlaces intermoleculares débiles dan sustancias moleculares orgánicas, tales como ceras y aceites, su carácter de masa blanda y sus puntos de fusión bajos (en los líquidos, las moléculas deben cesar el contacto más estructurado o orientado entre sí). Sin embargo, cuando los enlaces covalentes unen cadenas largas de átomos en moléculas grandes (como en polímeros como el nylon), o cuando los enlaces covalentes se extienden en redes a través de sólidos que no están compuestos de moléculas discretas (como diamante o cuarzo o los minerales de silicato en muchos tipos de roca), las estructuras resultantes pueden ser fuertes y duras, al menos en la dirección orientada correctamente con redes de enlaces covalentes. Además, los puntos de fusión de tales polímeros y redes covalentes aumentan enormemente.
En una vista simplificada de un enlace iónico , el electrón de enlace no se comparte en absoluto, sino que se transfiere. En este tipo de enlace, el orbital atómico externo de un átomo tiene una vacante que permite la adición de uno o más electrones. Estos electrones recién agregados potencialmente ocupan un estado de energía más bajo (efectivamente más cerca de una carga más nuclear) de lo que experimentan en un átomo diferente. Por lo tanto, un núcleo ofrece una posición más estrechamente unida a un electrón que otro núcleo, con el resultado de que un átomo puede transferir un electrón al otro. Esta transferencia hace que un átomo asuma una carga positiva neta, y el otro que asuma una carga neta negativa. El enlace luego los resultados de la atracción electrostática entre los átomos y los átomos se convierten en iones positivos o cargados negativamente. Los enlaces iónicos pueden verse como ejemplos extremos de polarización en enlaces covalentes. A menudo, tales enlaces no tienen una orientación particular en el espacio, ya que resultan de la atracción electrostática igual de cada ion a todos los iones que los rodean. Los enlaces iónicos son fuertes (y, por lo tanto, las sustancias iónicas requieren altas temperaturas para fundirse) pero también son frágiles, ya que las fuerzas entre iones son de corto alcance y no cubren fácilmente las grietas y fracturas. Este tipo de enlace da lugar a las características físicas de los cristales de sales minerales clásicas, como la sal de mesa.
Un tipo de unión menos mencionado es metálico vinculación. En este tipo de enlace, cada átomo en un metal dona uno o más electrones a un "mar" de electrones que residen entre muchos átomos metálicos. En este mar, cada electrón es libre (en virtud de su naturaleza de onda) para asociarse con muchos átomos a la vez. El enlace se produce porque los átomos de metal se cargan positivamente de algún modo debido a la pérdida de sus electrones, mientras que los electrones permanecen atraídos por muchos átomos, sin ser parte de ningún átomo dado. La unión metálica puede verse como un ejemplo extremo de deslocalización de electrones en un gran sistema de enlaces covalentes, en el que participa cada átomo. Este tipo de unión a menudo es muy fuerte (lo que resulta en la resistencia a la tracción de los metales). Sin embargo, los enlaces metálicos son de naturaleza más colectiva que otros tipos, por lo que permiten que los cristales de metal se deformen más fácilmente, porque están compuestos de átomos atraídos el uno al otro, pero no de ninguna manera particularmente orientada. Esto resulta en la maleabilidad de los metales. La nube de electrones en los enlaces metálicos causa la conductividad eléctrica y térmica característicamente buena de los metales, y también su brillante brillo que refleja la mayoría de las frecuencias de luz blanca.
Historia
Las primeras especulaciones sobre la naturaleza del vínculo químico , desde el siglo XII, suponían que ciertos tipos de especies químicas se unían por un tipo de afinidad química. En 1704, Sir Isaac Newton esbozó su teoría de vinculación atómica, en "Query 31" de su Opticks., donde los átomos se unen unos a otros por alguna "fuerza". Específicamente, después de reconocer las diversas teorías populares en boga en ese momento, de cómo los átomos se unieron, es decir, "átomos enganchados", "pegados entre sí por el reposo" o "unidos por movimientos conspirativos", Newton afirma que preferiría inferir de su cohesión, que "las partículas se atraen entre sí por alguna fuerza, que en contacto inmediato es extremadamente fuerte, a pequeñas distancias realiza las operaciones químicas, y alcanza no lejos de las partículas con algún efecto sensible".
En 1819, en los talones de la invención de la pila voltaica, Jöns Jakob Berzelius desarrolló una teoría de combinación química que enfatiza los caracteres electronegativos y electropositivos de los átomos que se combinan. A mediados del siglo XIX, Edward Frankland, FA Kekulé, AS Couper, Alexander Butlerov y Hermann Kolbe, basándose en la teoría de los radicales, desarrollaron la teoría de la valencia, originalmente llamada "poder de combinación", en la que los compuestos se unieron debido a un atracción de polos positivos y negativos. En 1916, el químico Gilbert N. Lewis desarrolló el concepto del enlace de pares de electrones, en el cual dos átomos pueden compartir de uno a seis electrones, formando así el enlace de un solo electrón, un enlace simple, un enlace doble o un enlace triple; en las propias palabras de Lewis "
Ese mismo año, Walther Kossel presentó una teoría similar a la de Lewis: solo su modelo suponía transferencias completas de electrones entre átomos y, por lo tanto, era un modelo de enlace iónico. Tanto Lewis como Kossel estructuraron sus modelos de vinculación sobre el de la regla de Abegg (1904).
Niels Bohr propuso un modelo del átomo y un modelo del enlace químico. De acuerdo con su modelo para una molécula diatómica, los electrones de los átomos de la molécula forman un anillo giratorio cuyo plano es perpendicular al eje de la molécula y equidistante de los núcleos atómicos. El equilibrio dinámico del sistema molecular se logra a través del equilibrio de fuerzas entre las fuerzas de atracción de los núcleos al plano del anillo de electrones y las fuerzas de repulsión mutua de los núcleos. El modelo de Bohr del enlace químico tuvo en cuenta la repulsión de Coulomb: los electrones en el anillo están a la distancia máxima el uno del otro.
En 1927, la primera descripción cuántica matemáticamente completa de un enlace químico simple, es decir, la producida por un electrón en el ion molecular de hidrógeno, H
2, fue derivado por el físico danés Oyvind Burrau. Este trabajo mostró que el enfoque cuántico de los enlaces químicos podría ser fundamental y cuantitativamente correcto, pero los métodos matemáticos utilizados no podrían extenderse a las moléculas que contienen más de un electrón. Un enfoque más práctico, aunque menos cuantitativo, fue presentado en el mismo año por Walter Heitler y Fritz London. El método de Heitler-Londres forma la base de lo que ahora se llama teoría del enlace de valencia. En 1929, Sir John Lennard-Jones introdujo la combinación lineal de la aproximación del método orbital molecular de orbitales atómicos (LCAO), que también sugirió métodos para derivar estructuras electrónicas de moléculas de F 2 (flúor) y O 2. (oxígeno) moléculas, a partir de principios básicos cuánticos. Esta teoría orbital molecular representaba un enlace covalente como un orbital formado por la combinación de los orbitales atómicos Schrödinger de mecánica cuántica que habían sido hipotetizados para electrones en átomos individuales. Las ecuaciones para unir electrones en átomos multielectrónicos no se pudieron resolver a la perfección matemática (es decir, analíticamente ), pero las aproximaciones para ellas todavía dieron muchas predicciones y resultados cualitativos buenos. La mayoría de los cálculos cuantitativos en la química cuántica moderna utilizan ya sea el enlace de valencia o la teoría de la órbita molecular como punto de partida, aunque un tercer enfoque, la teoría funcional de la densidad, se ha vuelto cada vez más popular en los últimos años.
2, fue derivado por el físico danés Oyvind Burrau. Este trabajo mostró que el enfoque cuántico de los enlaces químicos podría ser fundamental y cuantitativamente correcto, pero los métodos matemáticos utilizados no podrían extenderse a las moléculas que contienen más de un electrón. Un enfoque más práctico, aunque menos cuantitativo, fue presentado en el mismo año por Walter Heitler y Fritz London. El método de Heitler-Londres forma la base de lo que ahora se llama teoría del enlace de valencia. En 1929, Sir John Lennard-Jones introdujo la combinación lineal de la aproximación del método orbital molecular de orbitales atómicos (LCAO), que también sugirió métodos para derivar estructuras electrónicas de moléculas de F 2 (flúor) y O 2. (oxígeno) moléculas, a partir de principios básicos cuánticos. Esta teoría orbital molecular representaba un enlace covalente como un orbital formado por la combinación de los orbitales atómicos Schrödinger de mecánica cuántica que habían sido hipotetizados para electrones en átomos individuales. Las ecuaciones para unir electrones en átomos multielectrónicos no se pudieron resolver a la perfección matemática (es decir, analíticamente ), pero las aproximaciones para ellas todavía dieron muchas predicciones y resultados cualitativos buenos. La mayoría de los cálculos cuantitativos en la química cuántica moderna utilizan ya sea el enlace de valencia o la teoría de la órbita molecular como punto de partida, aunque un tercer enfoque, la teoría funcional de la densidad, se ha vuelto cada vez más popular en los últimos años.
En 1933, HH James y AS Coolidge llevaron a cabo un cálculo de la molécula de dihidrógeno que, a diferencia de todos los cálculos anteriores que usaban funciones solo de la distancia del electrón del núcleo atómico, usaba funciones que también agregaban explícitamente la distancia entre los dos electrones. Con hasta 13 parámetros ajustables obtuvieron un resultado muy cercano al resultado experimental para la energía de disociación. Las extensiones posteriores han utilizado hasta 54 parámetros y dieron un excelente acuerdo con los experimentos. Este cálculo convenció a la comunidad científica de que la teoría cuántica podía dar su acuerdo con el experimento. Sin embargo, este enfoque no tiene ninguna de las imágenes físicas del enlace de valencia y las teorías de orbitales moleculares y es difícil de extender a moléculas más grandes.
Bonos en fórmulas químicas
Debido a que los átomos y las moléculas son tridimensionales, es difícil utilizar un solo método para indicar orbitales y enlaces. En las fórmulas moleculares, los enlaces químicos (orbitales de unión) entre los átomos se indican de diferentes maneras dependiendo del tipo de discusión. Algunas veces, algunos detalles son descuidados. Por ejemplo, en química orgánica, a veces solo nos ocupamos del grupo funcional de la molécula. Por lo tanto, la fórmula molecular del etanol se puede escribir en forma conformacional, forma tridimensional, forma bidimensional completa (que indica cada enlace sin direcciones tridimensionales), forma bidimensional comprimida (CH 3 -CH 2-OH) , separando el grupo funcional de otra parte de la molécula (C 2 H 5OH), o por sus constituyentes atómicos (C 2 H 6 O), de acuerdo con lo discutido. A veces, incluso los electrones de capa de valencia que no se unen (con las direcciones aproximadas bidimensionales) están marcados, por ejemplo, para el carbono elemental . C. Algunos químicos también pueden marcar los respectivos orbitales, por ejemplo, el hipotético anión eteno ( \ C = C / ) que indica la posibilidad de formación de enlaces.
Fuertes enlaces químicos
| Longitudes de enlace típicas en pm y energías de enlace en kJ / mol. Las longitudes de enlace se pueden convertir a Å por división en 100 (1 Å = 100 μm). Datos tomados de la Universidad de Waterloo. | ||
| Enlace | Longitud (pm) | Energía (kJ / mol) |
|---|---|---|
| H - Hidrógeno | ||
| S.S | 74 | 436 |
| HO | 96 | 366 |
| H-F | 92 | 568 |
| H-Cl | 127 | 432 |
| C - Carbono | ||
| C-H | 109 | 413 |
| C-C | 154 | 348 |
| C-C = | 151 | |
| = C-C≡ | 147 | |
| = C-C = | 148 | |
| C = C | 134 | 614 |
| C≡C | 120 | 839 |
| C-N | 147 | 308 |
| CO | 143 | 360 |
| C-F | 134 | 488 |
| C-Cl | 177 | 330 |
| N - Nitrógeno | ||
| NUEVA HAMPSHIRE | 101 | 391 |
| N-N | 145 | 170 |
| N≡N | 110 | 945 |
| O - Oxígeno | ||
| O-O | 148 | 145 |
| O = O | 121 | 498 |
| F, Cl, Br, I - Halógenos | ||
| F-F | 142 | 158 |
| Cl-Cl | 199 | 243 |
| Br-H | 141 | 366 |
| Br-Br | 228 | 193 |
| I-H | 161 | 298 |
| I-I | 267 | 151 |
Los enlaces químicos fuertes son las fuerzas intramoleculares que mantienen unidos a los átomos en las moléculas. Un enlace químico fuerte se forma a partir de la transferencia o intercambio de electrones entre los centros atómicos y se basa en la atracción electrostática entre los protones en los núcleos y los electrones en los orbitales.
Los tipos de enlace fuerte difieren debido a la diferencia en electronegatividad de los elementos constituyentes. Una gran diferencia en la electronegatividad conduce a un carácter más polar (iónico) en el enlace.
Enlace iónico
La unión iónica es un tipo de interacción electrostática entre átomos que tienen una gran diferencia de electronegatividad. No existe un valor preciso que distinga el enlace iónico del enlace covalente, pero una diferencia de electronegatividad de más de 1,7 es probablemente iónica, y una diferencia de menos de 1,7 es probable que sea covalente. La unión iónica conduce a separar los iones positivos y negativos. Las cargas iónicas son comúnmente entre -3e a + 3e. La unión iónica ocurre comúnmente en sales metálicas como el cloruro de sodio (sal de mesa). Una característica típica de los enlaces iónicos es que las especies se forman en cristales iónicos, en los que ningún ion se empareja específicamente con ningún otro ion, en un enlace direccional específico. Por el contrario, cada especie de iones está rodeada por iones de la carga opuesta, y el espacio entre ella y cada uno de los iones cargados opuestamente cerca de él, es el mismo para todos los átomos circundantes del mismo tipo. Por lo tanto, ya no es posible asociar un ion con otro átomo único ionizado específico cerca de él. Esta es una situación diferente a la de los cristales covalentes, donde los enlaces covalentes entre átomos específicos todavía son discernibles desde las distancias más cortas entre ellos, medida a través de técnicas tales como la difracción de rayos X.
Los cristales iónicos pueden contener una mezcla de especies covalentes e iónicas, como por ejemplo sales de ácidos complejos, tales como cianuro de sodio, NaCN. La difracción de rayos X muestra que en NaCN, por ejemplo, los enlaces entre los cationes de sodio (Na) y los aniones de cianuro (CN) son iónicos , sin ion de sodio asociado con ningún cianuro en particular. Sin embargo, los enlaces entre los átomos C y N en el cianuro son del tipo covalente , de modo que cada carbono está fuertemente ligado a un solo nitrógeno, al que físicamente está mucho más cerca que a otros carbonos o nitrógenos en un cristal de cianuro sódico.
Cuando tales cristales se funden en líquidos, los enlaces iónicos se rompen primero porque no son direccionales y permiten que las especies cargadas se muevan libremente. De manera similar, cuando tales sales se disuelven en agua, los enlaces iónicos se rompen típicamente por la interacción con el agua, pero los enlaces covalentes continúan manteniéndose. Por ejemplo, en solución, los iones de cianuro, todavía unidos como iones CN individuales, se mueven independientemente a través de la solución, al igual que los iones sodio, como Na. En el agua, los iones cargados se separan porque cada uno de ellos se siente más atraído por un número de moléculas de agua que por el otro. La atracción entre los iones y las moléculas de agua en tales soluciones se debe a un tipo de enlace químico débil tipo dipolo-dipolo. En los compuestos iónicos fundidos, los iones se siguen atrayendo entre sí, pero no de forma ordenada o cristalina.
Enlace covalente
El enlace covalente es un tipo común de enlace, en el que dos o más átomos comparten electrones de valencia más o menos por igual. El tipo más simple y más común es un enlace simple en el que dos átomos comparten dos electrones. Otros tipos incluyen el enlace doble, el enlace triple, los enlaces de uno y tres electrones, el enlace de dos electrones de tres centros y el enlace de cuatro electrones de tres centros.
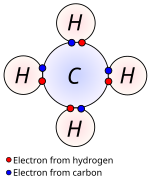
En los enlaces covalentes no polares, la diferencia de electronegatividad entre los átomos enlazados es pequeña, típicamente de 0 a 0.3. Los bonos dentro de la mayoría de los compuestos orgánicos se describen como covalentes. La figura muestra metano (CH 4 ), en el cual cada hidrógeno forma un enlace covalente con el carbono. Ver enlaces sigma y enlaces pi para LCAO-descripción de tal enlace.
Las moléculas que se forman principalmente a partir de enlaces covalentes no polares a menudo son inmiscibles en agua u otros disolventes polares, pero mucho más solubles en disolventes no polares tales como el hexano.
Un enlace covalente polar es un enlace covalente con un carácter iónico significativo. Esto significa que los dos electrones compartidos están más cerca de uno de los átomos, creando un desequilibrio de carga. Tales enlaces se producen entre dos átomos con electronegatividades moderadamente diferentes y dan lugar a interacciones dipolo-dipolo. La diferencia de electronegatividad entre los dos átomos en estos enlaces es de 0.3 a 1.7.
Bonos únicos y múltiples
Un enlace simple entre dos átomos corresponde al intercambio de un par de electrones. La densidad electrónica de estos dos electrones de enlace se concentra en la región entre los dos átomos, que es la cualidad definitoria de un enlace sigma.
Un doble enlace entre dos átomos se forma compartiendo dos pares de electrones, uno en un enlace sigma y otro en un enlace pi, con densidad de electrones concentrada en dos lados opuestos del eje internuclear. Un enlace triple consiste en tres pares de electrones compartidos, formando un sigma y dos enlaces pi.
Los enlaces cuádruples y superiores son muy raros y ocurren solo entre ciertos átomos de metales de transición.
Enlace covalente coordinado (enlace dipolar)
Un enlace covalente coordinado es un enlace covalente en el cual los dos electrones de enlace compartidos son del mismo átomo involucrado en el enlace. Por ejemplo, trifluoruro de boro (BF 3 ) y amoníaco (NH 3 ) de un aducto o complejo de coordinación F 3B ← NH 3 con un enlace B-N en el que un par solitario de electrones en N se comparte con un orbital atómico vacío en B. BF 3 con un orbital vacío se describe como un aceptor de par de electrones o ácido de Lewis, mientras que NH 3 con un par solitario que puede ser compartido se describe como un donante de par de electrones o base de Lewis. Los electrones se comparten aproximadamente a partes iguales entre los átomos en contraste con los enlaces iónicos. Tal unión se muestra con una flecha que apunta al ácido de Lewis.
Los complejos de metales de transición están generalmente unidos por enlaces covalentes coordinados. Por ejemplo, el ion Ag reacciona como un ácido de Lewis con dos moléculas de la base de Lewis NH 3 para formar el complejo Ag ion (NH 3 ) 2 , que tiene dos Ag ← N enlaces covalentes coordinados.
Unión metálica
En la unión metálica, los electrones de enlace se deslocalizan sobre una red cristalina de átomos. Por el contrario, en los compuestos iónicos, las ubicaciones de los electrones de unión y sus cargas son estáticas. El movimiento libre o la deslocalización de los electrones de enlace conduce a propiedades metálicas clásicas como el brillo (reflectividad de la luz de la superficie), la conductividad eléctrica y térmica, la ductilidad y la alta resistencia a la tracción.
Enlace intermolecular
Hay cuatro tipos básicos de enlaces que se pueden formar entre dos o más (por lo demás, no asociadas) moléculas, iones o átomos. Las fuerzas intermoleculares provocan que las moléculas sean atraídas o rechazadas entre sí. A menudo, estos definen algunas de las características físicas (como el punto de fusión) de una sustancia.
- Una gran diferencia en electronegatividad entre dos átomos enlazados causará una separación de carga permanente, o dipolo, en una molécula o ion. Dos o más moléculas o iones con dipolos permanentes pueden interactuar dentro de las interacciones dipolo-dipolo. Los electrones de enlace en una molécula o ion estarán, en promedio, más cerca del átomo más electronegativo con mayor frecuencia que el menos electronegativo, dando lugar a cargas parciales en cada átomo y causando fuerzas electrostáticas entre moléculas o iones.
- Un enlace de hidrógeno es efectivamente un fuerte ejemplo de una interacción entre dos dipolos permanentes. La gran diferencia en electronegatividades entre el hidrógeno y cualquiera de los átomos de flúor, nitrógeno y oxígeno, junto con sus pares de electrones solitarios causa fuertes fuerzas electrostáticas entre las moléculas. Los enlaces de hidrógeno son responsables de los puntos de alto punto de ebullición del agua y el amoníaco con respecto a sus análogos más pesados.
- La fuerza de dispersión de Londres surge debido a dipolos instantáneos en átomos vecinos. Como la carga negativa del electrón no es uniforme en todo el átomo, siempre hay un desequilibrio de carga. Esta pequeña carga inducirá un dipolo correspondiente en una molécula cercana; causando una atracción entre los dos. El electrón luego se mueve a otra parte de la nube de electrones y la atracción se rompe.
- Se produce una interacción catión-pi entre un enlace pi y un catión.
Teorías de enlace químico
En el límite (irreal) del enlace iónico "puro", los electrones están perfectamente localizados en uno de los dos átomos del enlace. Tales enlaces pueden ser entendidos por la física clásica. Las fuerzas entre los átomos se caracterizan por potenciales electrostáticos continuos isotrópicos. Su magnitud es en proporción simple a la diferencia de carga.
Los enlaces covalentes se entienden mejor mediante la teoría del enlace de valencia o la teoría del orbital molecular. Las propiedades de los átomos involucrados pueden entenderse usando conceptos tales como el número de oxidación. La densidad de electrones dentro de un enlace no se asigna a átomos individuales, sino que se deslocaliza entre átomos. En la teoría del enlace de valencia, los dos electrones en los dos átomos se acoplan con la fuerza de enlace en función de la superposición entre ellos. En la teoría de orbitales moleculares, la combinación lineal de orbitales atómicos (LCAO) ayuda a describir las estructuras orbitales moleculares deslocalizadas y las energías basadas en los orbitales atómicos de los átomos de donde provienen. A diferencia de los enlaces iónicos puros, los enlaces covalentes pueden tener propiedades anisotrópicas dirigidas. Estos pueden tener sus propios nombres, como sigma bond y pi bond.
En el caso general, los átomos forman enlaces que son intermedios entre iónicos y covalentes, dependiendo de la electronegatividad relativa de los átomos involucrados. Este tipo de enlace a veces se llama polar covalente.